 无机非金属材料的主角硅教案.docx
无机非金属材料的主角硅教案.docx
- 文档编号:13772583
- 上传时间:2023-06-17
- 格式:DOCX
- 页数:15
- 大小:38.13KB
无机非金属材料的主角硅教案.docx
《无机非金属材料的主角硅教案.docx》由会员分享,可在线阅读,更多相关《无机非金属材料的主角硅教案.docx(15页珍藏版)》请在冰点文库上搜索。
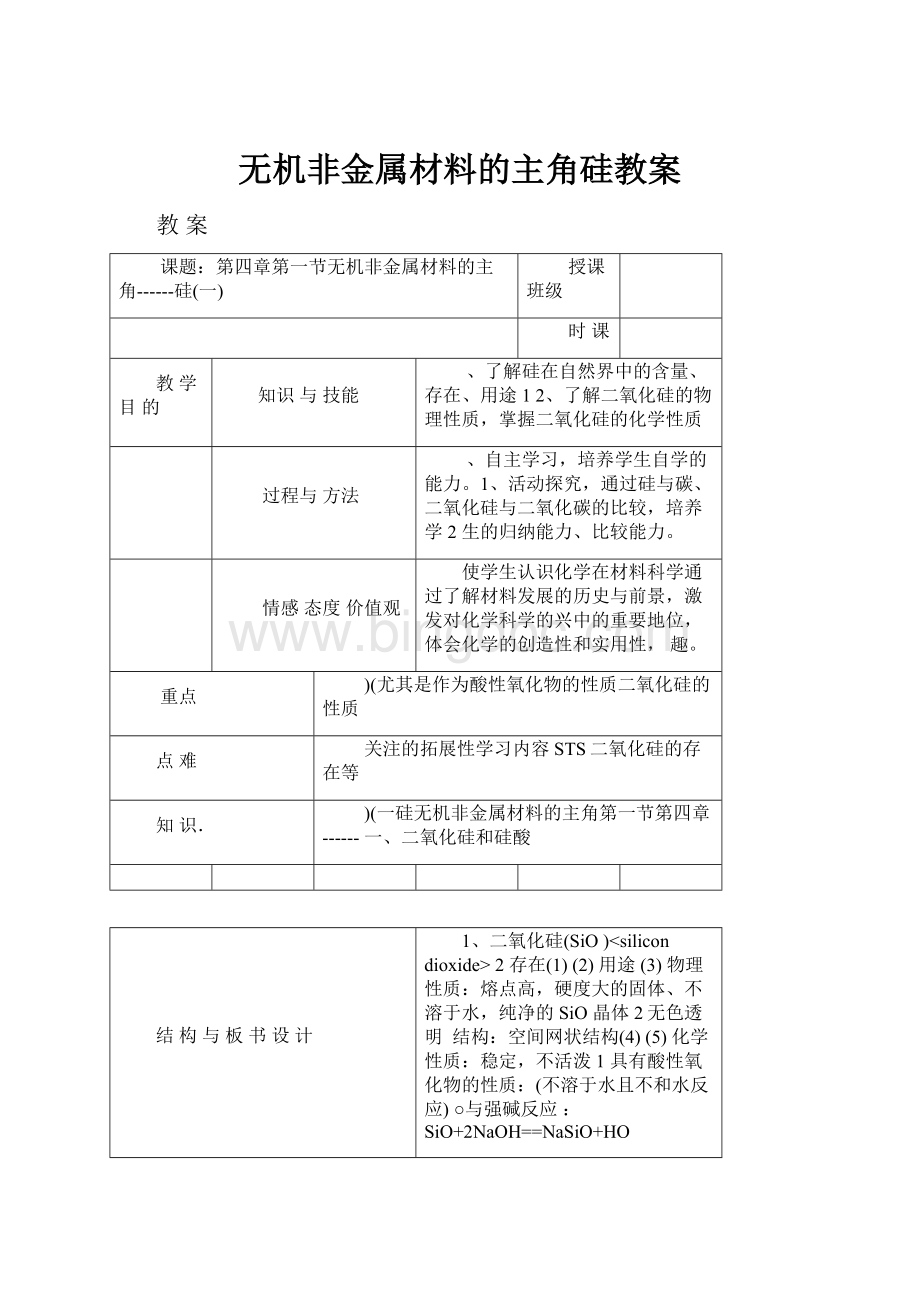
无机非金属材料的主角硅教案
教案
课题:
第四章第一节无机非金属材料的主角------硅
(一)
授课班级
时课
教学目的
知识与技能
、了解硅在自然界中的含量、存在、用途12、了解二氧化硅的物理性质,掌握二氧化硅的化学性质
过程与方法
、自主学习,培养学生自学的能力。
1、活动探究,通过硅与碳、二氧化硅与二氧化碳的比较,培养学2生的归纳能力、比较能力。
情感态度价值观
使学生认识化学在材料科学通过了解材料发展的历史与前景,激发对化学科学的兴中的重要地位,体会化学的创造性和实用性,趣。
重点
)(尤其是作为酸性氧化物的性质二氧化硅的性质
点难
关注的拓展性学习内容STS二氧化硅的存在等
知识.
)(一硅无机非金属材料的主角第一节第四章------一、二氧化硅和硅酸
结构与板书设计
1、二氧化硅(SiO)
(1)
(2)用途(3)物理性质:
熔点高,硬度大的固体、不溶于水,纯净的SiO晶体2无色透明结构:
空间网状结构(4)(5)化学性质:
稳定,不活泼1具有酸性氧化物的性质:
(不溶于水且不和水反应)○与强碱反应:
SiO+2NaOH==NaSiO+HO
2232高温+CaOCaSiO与碱性氧化物反应:
SiO32
2与HF的反应:
SiO+4HF==SiF↑+2HO○224)SiO、硅酸(H232硅酸是一种弱酸,它不溶于水,不能使指示剂变色,是一种白色粉末状的固体。
NaSiO+2HCl==2NaCl+HSiO↓3223↓SiO+HSO==NaSO+HSiONa32424232.
↓+HSiO+CO+HO==NaCONaSiO32222332△HO+SiOHSiO2322
教学过程
教学步骤、内容
教学方法、手段、师生活动
我们生成的地球,它坚硬的地壳是由什么构成的?
[引入]岩石,构成岩石的主要成分是硅酸盐及硅的氧化物。
一提到硅,同学们又能想到什么呢?
[问]硅谷:
美国新兴的高技术产业开发区,电子技术研究中心,计算.,位于加利福尼亚州圣弗朗西斯科南端机生产的重要基地半导体:
单晶硅是半导体器材的核心材料,硅半导体是集成电路以硅仍然会占半导体材料的95%估计在21世纪,的主要材料,.上沙子、石英、水晶:
主要成分是硅的氧化物光导纤维:
从石英玻璃熔融体中,拉出直径为100微米的细丝.再把千百根光导纤维组合并增强处理,就制成成光缆,其优点:
.成本低保密性好,输送距离长质轻,体积小,,[导入]从古至今,在无机非金属材料中,硅一直都在扮演着------就让我们一同来研究一下硅的氧化物今天,主要的角色。
.
配以多媒体图片从感性上让学生接触要学习的内容,激起学生学习的兴趣。
联系生活,激发求知欲。
图片呈现,直观、深刻,加深认识。
抽象思维,初步建立SiO空间2立体结构。
通过视频呈现,使学
。
二氧化硅及硅酸和硅酸盐的性质)硅(一[板书]第四章第一节无机非金属材料的主角------[讲]硅在地壳中含量丰富,仅次于氧,排在第二位,约占。
26.3%元素周期表[投影]位于周期表中的第四长列上的是碳族,这一族可谓是豪[讲]门望族。
其中具有代表性的是其中的两位兄长。
碳,形成了无数种构成人类和其它地球生物等的有机物,“统治了有机界”。
其构成的煤、石油等有机化产品和材料是现代化的基石。
而它的弟弟------硅,地壳质量的约90%,构成了地壳大部分岩石、沙子和土壤,“统治了地壳”,而当今硅酸盐工业的陶瓷、玻璃、水泥等使人类生活日新月异。
的原子结构简图,并由此分析:
硅Si[思考与交流]画出C、的化学性质活不活泼,为什么?
硅的化合价主要是多少?
[讲]Si原子最外层有四个电子,既不易失电子,也不易得电子,所以,硅的化学性质不活泼。
主要形成四价的化合物。
硅是一种亲氧元素,在自然界它总是与氧相互化合。
所以在氧化气氛包围的地球上,硅主要以熔点很高的氧化物及硅酸盐的形式存在。
常温下,单质碳、硅的化学性质都不活泼,为什么碳[思考]
生对SiO的结2构的理解更深刻。
提高学生信息处理能力,提高学生科学精神BBDCBCD
在自然界中有稳定的单质(金刚石)存在,而硅却没有,说明了什么?
单质硅的化学性质虽然稳定,但硅是一种亲氧元素,硅原子和氧原子的结合非常牢固,形成的二氧化硅或硅酸盐中的硅氧化学键非常牢固,硅氧键一旦形成就很难被破坏,所以,自然界中硅都是以二氧化硅或硅酸盐的形式存在,没有游离态的硅。
下面我们首先来研究一下二氧化硅的性质和用途。
[过][板书]一、二氧化硅和硅酸
1、二氧化硅(SiO)
(1)
[讲]SiO是硅的重要化合物。
地球上存在的天然二氧化硅约2占地壳质量的12%,其存在形态有结晶形和无定形两大类,通称硅石。
并展示水晶、玛瑙、石英坩埚、一段光缆[投影][讲]水晶是自然界中六方柱状的透明晶体,玛瑙的成分也是SiO,它们除了一些常见的可作饰物等用途外,SiO在工业上22用途也非学广泛,例如,以石英为材料而制成的纤维在电信行业的应用等。
用途
(2)[板书]
结晶形:
玛瑙、石英、水晶
硅石
无定形:
硅藻土
[投影小结]①、制光导纤维②、石英玻璃制化学仪器③、石英表、石英钟④、水晶制光学仪器和工艺品⑤、玛瑙制精密轴承和装饰品[讲]结合已有的关于水晶、沙子主要成分也是SiO的知识,2进行比较研究CO的物理性质有哪些,注意与思考一下,SiO22[板书](3)物理性质:
熔点高,硬度
大的固体、不溶于水,纯净的SiO晶体2无色透明
[思考]为什么SiO与CO的性质上有着22这么大的差别呢?
[SiO]四面体结[讲]主要取决于结构的不同。
CO是C与O通过化学键所连接2四面体结构O—SiO的分子结构,而Si是2.
硅氧四面体结构[投影][讲][SiO]四面体:
每1个Si原子周围结合4个O原子,Si4在中心,O在四个顶角.同时每1个O原子周围结合2个Si原子相结合。
二氧化硅中氧原子与硅原子个数比为2:
1,通常用.来表示二氧化硅的组成SiO2结构:
空间网状结构(4)[板书][讲]我们说,结构决定性质,SiO的网状结构不仅决定了其2物理性质的特殊性,还决定了其化学性质的稳定性。
[板书](5)化学性质:
稳定,不活泼
1具有酸性氧化物的性质:
(不溶于水且不和水反应)○与强碱反应:
SiO+2NaOH==NaSiO+HO
2223高温CaSiO与碱性氧化物反应:
SiO+CaO32
[讲]SiO除了具有酸性氧化物的通用性之外,还具有特性。
2比如酸性氧化物一般不与酸反应,而SiO却能与HF反应,这2也是工业上雕刻玻璃的反应原理2与HF的反应:
SiO+4HF==SiF↑+2HO[板书]○224[讲]除此之外,SiO在制水泥、玻璃、纯硅时,还有一些特2殊反应[投影小结]
高温)(3弱氧化性:
SiO+2C工业上制粗硅Si+2CO↑○2
高温↑NaSiO+CO与某些盐反应:
4NaCO+SiO○232223
高温)工业上制玻璃的主要反应↑CaCO+SiO(CaSiO+CO2332
、实验室为什么不用玻璃瓶盛装氢氟酸?
1[思考与交流]HF能腐蚀玻璃,因此,盛装氢氟酸不能用玻璃试剂瓶而要用塑料瓶。
2、实验室盛装NaOH溶液的试剂瓶为什么用橡胶塞而不用玻璃塞?
NaOH溶液能与玻璃中的SiO反应生成NaSiO,使瓶塞部322分粘结而无法打开。
因此盛装NaOH溶液的试剂瓶不能用玻璃塞而要用橡胶塞。
[过]刚才我们提到SiO不能溶于HO得到相应的酸,但它对22应的酸叫硅酸,那么硅酸是一种怎样制得的酸呢?
)(HSiO[板书]2、硅酸32[讲]HSiO是一种比HCO还要弱的酸,它不溶于水,不能使3223指示剂褪色,是一种白色粉末状的固体。
[板书]硅酸是一种弱酸,它不溶于水,不能使指示剂变色,是一种白色粉末状的固体。
[问]SiO不溶于水且不和水反应,那么要如何制备硅酸呢?
2.
的方法来设想一下?
结合初中制备CO2[讲]初中制备CO是利用碳酸盐与强酸反应,是强酸制弱酸2的原理。
HSiO也是一种很弱的酸,我们是否也可以用硅酸盐32来制备呢?
4-1P76实验[投影实验]溶液中滴入酚酞,再滴入稀盐酸SiO4-1:
向饱和Na实验32[问][板书]Na[讲]度较大时,则形成软而透明的、胶冻状的硅酸凝胶。
硅酸凝胶经干燥脱水就形成硅酸干胶,称为“硅胶”。
硅胶多孔,吸附水分能力强,
现象
滴入酚酞溶液显红色,再滴入盐酸红色消失,并有透明胶状物质生成
结论
NaSiO溶液呈碱性,与酸反应生成了HSiO且3223难溶于水HSiO32
化学方程式
+2NaCl↓SiONa+2HCl==HSiO3223
会有什么现象呢?
溶液中滴加HSOSiO若改向Na4322NaSiO+2HCl==2NaCl+HSiO↓3232↓SiOSOSOSiO+H==Na+H32232424所生成的硅酸逐渐聚合而形成胶体-硅酸溶胶,硅酸浓瓶装药品等的干燥剂,常用做实验室和袋装食品、
也可以用作催化剂的载体。
如果对硅酸加热,其可以分解生成SiO[讲]2△HO+SiO[板书]HSiO2223
[活动与探究]硅酸是一种比碳酸还要弱的酸,请利用中学实验室常见的仪器及药品,设计一个简单实验,证明硅酸的酸性比碳酸弱,并完成一份实验报告。
[分析]利用CO溶于水产生HCO,而HCO的酸性比HSiO的3233222的溶液中。
SiO通入到Na酸性强,可以将CO322↓SiO+HO==NaCO+H[板书]NaSiO+CO32222323[总结]本节课我们学习了一种重要的非金属元素硅的化合物SiO和HSiO,了解了SiO的重要性质及用途。
知道了晶莹透2223明的水晶、五彩斑斓的玛瑙与普通沙子的化学成分并没有什么两样。
知道了SiO在当前信息时代、IT产业中的重要作用。
化2学知识可以帮助我们认识,了解世界,我们也可以用学过的知识进行发明、创造,造福人类。
[自我评价])1、制造光导纤维的主要原料是(硅酸钠D.二氧化硅C.石墨B.A.晶体硅)、下列说法正确的是(2.
溶于水显酸性.SiOA2硅酸钠的水溶液)可得硅酸通入水玻璃(B.CO2是酸性氧化物,它不溶于任何酸.SiOC2分子晶体中不存在单个SiOD.SiO22()不能用玻璃瓶来盛装的是3、下列物质中,A.烧碱溶液B.浓硫酸C.氢氟酸D.碳酸钠溶液)最适宜的试剂是(SiO中的CaO杂质,4、要除去2A.纯碱溶液B盐酸C硫酸D苛性钠溶液)、加热熔融烧碱时应使用下列哪种坩埚(5A.石英坩埚B.普通玻璃坩埚C.铁坩埚D.陶瓷坩埚6、CO通入下列各溶液中,不可能产生沉淀的是2()饱和碳酸钠溶液B石灰水A
氯化钙溶液硅酸钠溶液DC
(BC)若最终产生沉淀的是
:
教学回顾
案教
课题:
第四章第一节无机非金属材料的主角------硅
(二)
授课班级
时课
教学目的
知识与技能
、了解硅酸盐、硅的主要性质1、认识硅酸盐、硅等在生产、信息技术、材料科学等领域的应用2
过程与方法
通过硅与碳的比较学习,引导学生学会运用对比的方法来认识物质。
情感态度价值观
通过对硅酸盐材料及硅的用途学习,使学生了解新型无机非金属材料,培养学生热爱科学的情感。
点重
硅、硅酸盐的丰富性和多样性
点难
通过学习,掌握研究非金属元素单质及化合物的一般方法
知识.
二、硅酸盐(silicate)
、定义:
硅酸盐是由硅、氧、金属所组成的化合物的总称。
1
结构与板书设计
2、硅酸钠
(1)物理性质:
白色固体,易溶于水,水溶液俗称水玻璃或泡花碱,是一种泡花碱
(2)化学性质:
相对稳定,不能燃烧,不易被腐蚀,热稳定性强3、表示方法:
原则:
金属氧化物(较活泼------较不活泼)12写成氧化物的形式方法:
○找组成元素○34检查有无遗漏○○原子个数比不变
三、硅(silicon)单质
、存在形态:
有晶体硅和无定形硅两种同素异形体1、晶体结构:
正四面体形23、物理性质:
灰黑色具有金属光泽的固体、熔点高、硬度大、质脆、导电性介于导体和绝缘体之间,是好的半导体材料。
4、化学性质
常温下的反应:
(1)
↑+2HSi+2F==SiFSi+4HF==SiF↑2244↑SiO+2HSi+2NaOH+HO==Na2223
(2)高温下的反应:
高温高温SiClSi+OSiOSi+2Cl4222
5、硅的制备
(1)工业上制粗硅
高温Si+2CO↑SiO+2C2
石英砂焦炭电炉中粗硅
(2)由粗硅制纯硅
高温高温Si+4HCl+2HSiClSi+2ClSiCl2244
教学过程
教学步骤、内容
教学方法、手段、师生活动
[思考]SiO与CO在物理、化学性质方面有哪些相似性和不同之22处[投影回顾]
[回顾]事实上,在自然界中,硅酸盐是构成地壳岩石的主要成分,大多数硅酸盐是不溶于水的。
自然界中存在的各种天然硅酸盐矿物约占地壳总质量的[板书]二、硅酸盐1[讲]硅酸盐是硅酸钠,下面我们主要研究一下硅酸钠的性质.
CO2
SiO2
物理性质
无色无味气体,熔沸点都很低,微溶于水,存在于空气中
灰黑色固体,熔沸点都很高,不溶于水,存在于岩石中,俗名硅石、石英、水晶,纤维、玻璃、硅藻土中都大量含有
化学性质
碱和氧性化物
+CaO==CaCOCO32
高温+COCaSiOSiO322
和碱
+HOCOCO+2NaOH==Na2223
OSiO+H+2NaOH==NaSiO2322
和酸
--------
O+2H↑SiO+4HF==SiF242
和水
COCO+HO===H3222
--------
上节课我们提到,用可溶性硅酸盐NaSiO来制备HSiO。
3322。
5%(silicate)、定义:
硅酸盐是由硅、氧、金属所组成的化合物的总称。
硅酸盐结构复杂,一般不溶于水,性质很稳定。
最简单的
[板书]2、硅酸钠
(1)物理性质:
白色固体,易溶于水,水溶液俗称水玻璃或泡花碱,是一种泡花碱
、4-2P77实验[投影实验]饱和溶液SiO放入放入蒸馏水Na32当水分蒸发后不易燃烧现象当水分蒸发后燃烧用水玻璃浸泡过的木材或织物可防火结论[板书]
(2)化学性质:
相对稳定,不能燃烧,不易被腐蚀,
热稳定性强
[讲]硅酸盐的种类很多,结构复杂,为了方便记忆和计算,常用氧化物的形式表示硅酸盐的组成[板书]3、表示方法:
原则:
金属氧化物(较活泼------较不活泼)
12写成氧化物的形式找组成元素○方法:
○
34检查有无遗漏原子个数比不变○○[投影]例、请用氧化物的形式表示下列硅酸盐的组成:
————————————SiONa硅酸钠()32.
————————————)镁橄榄石(MgSiO42————————————}O{Al(Si)(OH)高岭土4225[讲]硅酸盐材料具有很多优良的性能,为我们的生活、为人类的科技进步作出了很大的贡献。
受传统陶瓷某些特殊性能的启发,科技工作者在此基础上进行了一次又一次的创新,又研制出了许多种组成不同、性能更特殊的新型陶瓷。
请大家阅读教材P77上的科学视野。
传统硅酸盐材料:
[投影]陶瓷:
日用器皿、建筑饰材、卫生洁具
(1)
玻璃:
(2)
水泥:
以黏土和石灰石为主要原料(3)
具有特殊功能的含硅物质:
碳化硅(金刚砂)
(1)
硅钢:
导磁性良好,用作变压器铁芯
(2)
硅橡胶(3)
分子筛:
具有均匀微孔结构的铝硅酸盐(4)
生物陶瓷:
人造骨(5)
虽然硅的化合物很多,随处可见,而且从远古时期人类就[过]
已经学会加工和使用陶瓷,但是硅的单质却到很晚------18世纪上半叶才制备出来。
硅别看起来灰溜溜的,它自己及化合物的作用却大得很,大到高科技领域,小到我们的周围,到处都有Si及其化合物的踪影,当今电子工业的飞速发展,更是人们对Si的性质的认识息息相关,及其化合物的有关知识。
本节我们就来学习Si[板书]三、硅(silicon)单质
、存在形态:
有晶体硅和无定形硅两种同素异形体1的结构模型Si展示晶体Si和晶体[投影]、晶体结构:
正四面体形2[板书][讲]晶体Si的结构类似于金刚石的正四面体型,因此物理性质与金刚石类似。
[板书]3、物理性质:
灰黑色具有金属光泽的固体、熔点高、硬是好的半导体材料。
导电性介于导体和绝缘体之间,度大、质脆、[讲]因为Si在元素周期表中的位置仅次于金属与非金属分界线附近,因此硅有些性质与金属相似。
硅的化学性质不活泼,常温下硅的化学性质很稳定,除F、HF和NaOH外,Si不跟其他物质2起反应。
、化学性质4[板书]
(1)常温下的反应:
Si+2F==SiF42↑Si+4HF==SiF↑+2H24↑+2HO==NaSiOSi+2NaOH+H2223等非金属单质发生反应能与SiO2[讲]在高温下,[板书]
(2)高温下的反应:
高温SiOSi+O22
高温SiClSi+2Cl42
[讲]硅可用来制造集成电路、晶体管、硅整流器等半导体器件,还可以制成太阳能电池,可制成有良好导磁性、耐酸性的合金。
半导体晶体管及芯片的出现,促进了信息技术革命。
请大家阅读教上的内容,了解一下硅的用途。
材P79-80[投影小结]1○信息技术的关健材料,——半导体、晶体管、芯片。
2○半导体性能——将太阳能转换为光能的重要材料——光电池
3○硅合金、硅的制备5[板书]
(1)工业上制粗硅
高温Si+2CO↑SiO+2C2
石英砂焦炭电炉中粗硅
(2)由粗硅制纯硅
高温SiClSi+2Cl42
高温Si+4HCl
+2HSiCl24
[总结]本节课我们学习了硅酸盐的重要用途及性质,了解了硅酸钠的特性------耐火。
知道了Si单质的重要用途。
从结构上、从周期表的位置,进一步理解了Si的性质。
21世纪人类所面临的重大问题之一是能源危机。
而从书上我们了解到Si是具发展前景的新能源材料。
同学们,随着人类对Si及其化合物的认识越来越深刻,随着科学技术的不断发展,我们有理由相信Si及其化合!
物对人类作出更大的贡献,给人类带来更大的惊喜[自我评价]
(C)1、下列关于硅的说法不正确的是、硅是非金属元素,它的单质是灰黑色,有金属光泽的固体A是良好的半导体材料。
硅的导电性能介于导体和绝缘体之间,、B、硅的化学性质不活泼,常温下不与任何物质反应C.
、加热到一定温度时,硅能与氧气、氯气等非金属反应D(AD)、下列关于碳和硅的叙述中,不正确的是2、氧化物都能与氢氧化钠溶液反应A、单质在加热时都能跟氧气反应B、氧化物溶于水都生成相应的酸C、碳和硅两种元素都有同素异型体D
:
教学回顾
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 无机 非金属材料 主角 教案
 冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 #电控发动机的故障诊断与排除.docx
#电控发动机的故障诊断与排除.docx
 班主任治班方略.pptx
班主任治班方略.pptx
