 水质分析常用仪器一览表.docx
水质分析常用仪器一览表.docx
- 文档编号:16088666
- 上传时间:2023-07-10
- 格式:DOCX
- 页数:13
- 大小:67.34KB
水质分析常用仪器一览表.docx
《水质分析常用仪器一览表.docx》由会员分享,可在线阅读,更多相关《水质分析常用仪器一览表.docx(13页珍藏版)》请在冰点文库上搜索。
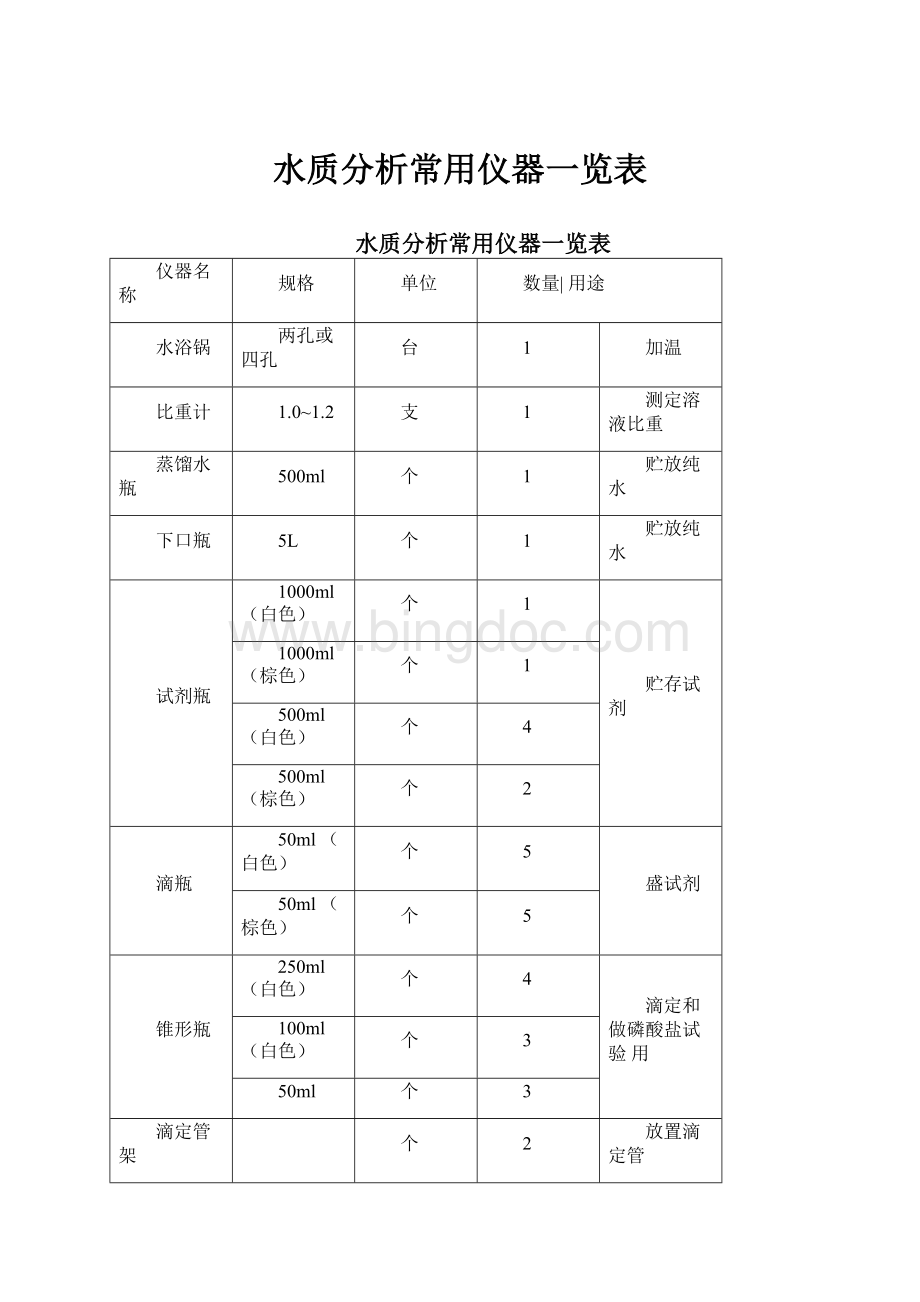
水质分析常用仪器一览表
水质分析常用仪器一览表
仪器名称
规格
单位
数量|用途
水浴锅
两孔或四孔
台
1
加温
比重计
1.0~1.2
支
1
测定溶液比重
蒸馏水瓶
500ml
个
1
贮放纯水
下口瓶
5L
个
1
贮放纯水
试剂瓶
1000ml(白色)
个
1
贮存试剂
1000ml(棕色)
个
1
500ml(白色)
个
4
500ml(棕色)
个
2
滴瓶
50ml(白色)
个
5
盛试剂
50ml(棕色)
个
5
锥形瓶
250ml(白色)
个
4
滴定和做磷酸盐试验用
100ml(白色)
个
3
50ml
个
3
滴定管架
个
2
放置滴定管
酸式滴定管
25ml(白色)
支
1
酸性、中性、氧化性溶液。
25ml(棕色)
支
1
碱式滴定管
25ml(白色)
支
2
碱性、无氧化性溶液
25ml(棕色)
支
2
微量滴定管
2~5ml(白色)
支
1
—测定软水硬度
容量瓶
250ml、100ml、
个
各2
配制溶液
单刻度移液管
25ml、5ml
支
各2
准确量取溶液
复刻度移液管
10ml、5ml、2ml、1ml
支
各1
准确量取溶液
量筒
500ml、100ml
个
各1
量取一般溶液
洗耳球
中号
个
2
吸取溶液
药勺
牛角或不锈钢
个
4
取固体药品
玻璃沸珠
袋
1
溶液加热时用
PH试纸
0~14
本
5
实验溶液酸碱性
PH计
PHS-250.00~14.000~±1999
台
1
准确测量溶液酸碱性
电导率仪
20us~20ms
台
1
准确测量溶液电导率
721分光光度计
台
1
测定磷酸盐含量
比色管
50ml
支
3
测磷酸盐、铜、铁离子用
滤纸
中速
盒
1
过滤溶液用
比色皿
10mm
盒
1
测吸光度用
20mm
盒
1
塑料吸管
1ml
袋
1
吸溶液用
可调电炉
220V1000W
循环冷却水系统日常监测
所需分析化验设备、器皿、试剂
、设备:
购买)
个)
器皿:
棕色1支。
2、锥形瓶:
250ML6个,100ML3个
3、大肚移液管:
100ML1支,50ML1支,25ML1支,20ML1支,10ML1支。
4、直筒移液管:
5ML6支,2ML2支,1ML2支。
5、烧杯:
1000ML1个,500ML1个,100ML6个。
6、容量瓶:
2000ML1个,1000ML2个,500ML2个,250ML4个,
100ML2个。
7、比色管:
50ML7支。
8、比色管架(9-12孔):
一个.
9、玻璃棒:
3支。
10、温度计:
(0C~100C)2支。
11、滴瓶:
125ML:
棕色3个,无色1个,60ML无色2个。
12、称量瓶:
25X25MM=2个,50X30MM=1个。
13、量筒:
100ML=1个,50ML=1个。
14、磨口瓶:
500ML棕色小口2个、无色小口2个,250ML无色小口6个、1000ML无色小口1个。
15、标准溶液储存瓶:
2000ML无色1个、1000ML无色2个、棕色1个。
16、玻璃漏斗100ML1个,70ML2个。
17、其他:
洗瓶:
500ML3个,洗耳球:
2个,药勺:
4个、剪子1把,滴定管刷1个,烧杯刷2人,移液管架1个,瓷研钵1个,瓷坩锅50ML2个,直尺(0~50cm)1把,耐酸手套1副试剂标签纸:
大5张、小5张、滴管3~5个。
三、试剂:
1氯化氨、2浓氨水、3络黑T、4氢氧化钾、5三乙醇胺、6浓盐酸、7浓硫酸、8浓硝酸、9钼酸胺、10抗坏血酸、11酒石酸锑钾、12甲酸、13过硫酸铵、14无水碳酸钠(基准)、15酚酞、16甲基橙、17氢氧化钠、18硝酸汞、19二苯卡巴肼、20溴酚兰、21凡士林、22氯化钾、23钙试剂羧酸钠、24乙二氨四乙酸二钠、25锌粒(或基准氧化锌)、26硫脲、27磷酸二氢钾等二十七种各一瓶。
氯化钠:
基准一瓶,分析纯一瓶,共二瓶。
乙醇:
二瓶。
硅胶:
三瓶。
中速滤纸15cm五盒。
注:
1、无甲基橙时,可用溴甲酚绿、甲基红替代。
注:
2、无硝酸汞、二苯卡巴肼、溴酚兰、可采购络酸钾、硝酸银、硝酸铜各一瓶(测CL-改用银量法)说明:
本清单是运行循环冷却水系统日常监测必不可少的量。
如企业内部有多个实验室能自行调节或存有备品、代用品时可以
不买。
(一)循环水及补充水水质分析方法
A1总硬度的测定
A1.1试剂及配制
A1.1.1CEDT=0.05mol/L乙二胺四乙酸二钠标准溶液的配制与标定
A1.1.1.1配制
称取20g乙二胺四乙酸二钠溶于高纯水中,摇均。
A1.1.1.2标定
称取800乜灼烧恒重的基准氧化锌2g(精确到0.0002g),用少许水湿润,加盐酸溶解,移入500m容量瓶中,稀释至刻度,摇均。
取上述溶液0mL加80mL除盐水,用10氨水中和至pH=~8,加5mLM-氯化铵缓冲溶液pH=10),加5滴0.5铬黑指示剂,用0.05mol/L乙二胺四乙酸二钠(EDTA溶液滴定至溶液由紫色变为纯蓝色。
乙二胺四乙酸二钠标准溶液的浓度按下式算:
m200.04m
CEdt=------——
VedtaM500Vedta81.3794
式中:
Cedt”-标定的乙二胺四乙酸二钠标准溶液的浓度moi/L
m--氧化锌的质量,g
81.3794--ZnO的摩尔质量,g/mol
0.04--500m中取20mL滴定,相当于m的0.04倍,
VEDTT-滴定氧化锌消耗所配EDTAS准溶液的体积,L
A1.1.2氨嶺化铵缓冲溶液:
(pH=10)
称取20g分析纯氯化铵溶于50mL蒸馏水中,加入100m分析纯浓氨水,用蒸馏水
稀释至1000mL摇匀。
A1.1.3铬黑T指示剂:
称取0.5g铬黑T,加入100g固体分析纯氯化钠放入研体中研磨均匀,放入小广口瓶中备用。
A1.2测定方法
A1.2.1取适量透明水样注于250mL锥形瓶中,用除盐水稀释至100mL加入5mL氨氯化铵缓冲溶液和铬黑T指示剂,在不断摇动下用GDT=0.05mol/LEDT标准溶液滴定至溶液由酒红色变为蓝色即为终点,记1EDTAS准溶液所消耗的体积V。
硬度(YD的含量按下式计算:
CEdtaXVedtaX2
YD=丸-^mm-/-——
Vs
CEDTAXVEDTA
或YD=XCPX00.09mg/Lf以CaCG计)
Vs
式中:
CEdt”—EDTA标准溶液的浓度,mol/L
Vedtf-滴定时所消耗EDTA标准溶液的体积,mL
Vs取水样的体积,mL
100.09碳酸钙的摩尔质量,g/moL
注:
A1.2.2水样硬度在0.001~0.5mmol/的测定
取100mL透明水样注于250mL锥形瓶中,加3mL氨亲化铵缓冲溶液及30mg铬黑T指示剂,在不断摇动下,用C/2EDT=Q0010mol/L标准溶液滴定至蓝色即为终点,记录所消耗的C/2EDT=0.0010mol/L标准溶液的体积。
A1.2.3若水样的酸度或碱度较高时,应先用).1mol/L的氢氧化钠溶液或0.1mol/L的盐酸中和后再加缓冲溶液。
A2钙离子的测定
A2.1试剂及配制
20%KOH溶液:
称20gKOH(分析纯)溶于100mL蒸馏水中。
1:
2三乙醇胺:
1体积的三乙醇胺与2体积的蒸馏水混匀。
1:
1盐酸溶液:
1体积的浓盐酸与1体积的蒸馏水混合。
钙黄绿素一酚酞指示剂:
称取).2g钙黄绿素(分析纯)^.07g酚酞(分析纯)置于玻璃研体中,加入已在105C干燥1小时的氯化钾(分析纯)20g,研细磨匀即可。
0.01mol/L的EDTA标准溶液。
A2.2测试方法
用移液管吸取适量水样于250mL的锥形瓶中,加入20%KOH溶液5mL,钙黄绿素—酚酞指示剂一小勺(约30mg,用EDTA标准溶液滴定至溶液绿色荧光消失即为终点(滴定时要以黑色为背景)记录所消耗的EDTA标准溶液的体积。
V>CX000
Ca+(以CaCQ计)=>00mg/L
Vs
式中:
V--滴定时所消耗的EDTA标准溶液的体积,mL
C--EDTA标准溶液的浓度,mol/L
Vs--所取水样的体积,mL
100.09--——Q的摩尔浓度,g/moL
A3镁离子的测定(计算法)
Mg2+(以CaCQ计)=总硬度钙硬
A4碱度的测定
A4.1概要
水的碱度是指水中含有能接受氢离子的物质的量,例如氢氧根、碳酸盐、重碳酸盐、磷酸盐、磷酸氢盐、硅酸盐、硅酸氢盐、亚硫酸盐、腐植酸盐和氮等,都是水中常见的碱性物质,他们都能与酸反应。
因此选用适宜的指示剂,以酸的标准溶液对它们进行滴定,便可测出水中碱度的含量。
碱度可以分为酚酞碱度和全碱度两种。
酚酞碱度是以酚酞作指示剂时所测出的量,其
终点的值为8.3。
全碱度是以甲基橙作指示剂时测出的量,终点的H值为4.2。
若碱度很小时,全碱度应以甲基红亚甲基蓝作指示剂,终点的pH为5.0。
A4.2试剂及配制
1%酚酞指示剂(以乙醇为溶剂)
甲基红亚甲基蓝指示剂:
准确称取0.125g甲基红和0.085g亚甲基蓝,在研体中研磨均匀
后,溶于100mL95汇醇中。
C1/2HSO=0.1000mol/l硫酸标准溶液。
A4.3测定方法
取适量水样于250mL锥形瓶中,加2~3滴1%酚酞指示剂,此时若溶液显红色,则
用C1/2HSC4=0.1mol/L标准溶液滴定至恰为无色,记录耗酸的体积/1,然后加入2滴甲基红亚甲基蓝指示剂,继续用上述硫酸标准溶液滴定至溶液由绿色变为紫色,记录第二次消耗酸的体积V2(不包括V1)。
A4.4碱度的计算
C1/2H2SQ4>V1>1000
酚酞碱度=---------->—.05~=C—22SOr—1>00.5mg/L
C1/2H2SQXV2X1000
全碱度=-50.05^=C-/22S€-
100
C1/2HSQ--硫酸标准溶液的浓度,mol/L
Vi、V2--两次滴定时所消耗硫酸标准溶液的体积,mL
A5氯化物的测定(硝酸银容量法)
A5.1概要
适用于测定氯化物含量为5~100mg/L的水样。
在中性或弱碱性溶液中,氯化银与硝酸银作用生成白色氯化银沉淀,过量的硝酸银与铬酸钾作用生成砖红色铬酸银沉淀,使溶液显橙色,即为滴定终点。
A5.2试剂及配制
A5.2.1氯化钠标准溶液(ImL含img氯离子):
取基准试剂或优级纯的氯化钠3~4g置于瓷坩埚内,于高温炉内升温至500C灼烧10分钟,然后放入干燥器内冷却至室温,准确称取1.648gR化钠,先溶于少量蒸馏水,然后稀释至I000mb
A5.2.2硝酸银标准溶液1mL相当于1mgCl):
称取5.0g硝酸银溶于1000mL蒸馏水中,以氯化钠标准溶液滴定,方法如下:
于三个锥形瓶中,用移液管分别注入10mL氯化钠标准溶液,再加入90mL蒸馏水及1.0mL10%勺铬酸钾指示剂,均用硝酸银标准溶液滴定至橙色,分别记录硝酸银标准溶液的消耗量V,以平均值计算,但三个平行试验数值间的相对误差应小于).25%另取100mL蒸馏水作空白试验,除不加氯化钠标准溶液外,其他步骤同上,记录硝酸银标准溶液的体积V1。
硝酸银标准溶液的浓度按下式计算:
10<1.0
T=m-g/m-L---
V-V1
式中:
V1--空白试验消耗硝酸银标准溶液的体积,mL
V--氯化钠标准溶液消耗硝酸银标准溶液的平均体积mL
10--氯-化-钠标准溶液体积,mL
1.0--氯-化-钠标准溶液的浓度,mg/mL
最后调整硝酸银标准溶液浓度,使其成为mL相当于ImgCl的标准溶液。
A5.2.3试剂
10%铬酸钾指示剂;1%酚酞指示剂;CNaoH=0.1mol/LC1/2HSQ=0.1mol/LA5.3测定方法
A5.3.1取适量水样于250mL锥形瓶中,加2~3滴1%酚酞指示剂,若显红色,即用硫酸溶液中和至无色;若不显红色,则用氢氧化钠溶液中和至微红色,然后用硫酸溶液滴回至无色,再加入1.0mL10%铬酸钾指示剂。
A5.3.2用硝酸银标准溶液滴定至橙色,记录硝酸银标准溶液的体积。
氯化物含量按下式计算:
VX1.0
TCl-=X-0--m-L
Vs
式中:
V--滴定水样消耗硝酸银标准溶液的体积,mL
1.0--硝酸银标准溶液的滴定度,1mL相当于ImgCl
Vs--水样的体积,mL
A5.4滴定水样时应注意的事项
A5.4.1当水样中氯离子含量大于100mg/L时,须按下表中规定定的体积取水样,用蒸馏水稀释至100mL后测定。
氯化物的含量和取水样的体积
水中Cl-含量,mg/L
101~200
201~400
401~1000
取水样体积,mL
50
25
10
A5.4.2当水样中硫离子(S2-)含量大于5mg/L,铁铝含量大于3mg/L或颜色太深时,应事先用过氧化氢作脱色处理(每升水加20mL),并煮沸10min后过滤。
如颜色依旧不消失,可在100mL水样中加1g碳酸钠然后蒸干,将干涸物用蒸馏水溶解后再进行测定。
A5.4.3若水样中氯离子含量小于5mg/L时,可将硝酸银标准溶液稀释为1mL相当于
0.5mgG后使用。
A5.4.4为了便于观察终点,可另取保100mL水样加班1mL10%铬酸钾指示剂作对照。
A5.4.5若水样混浊,应事先过滤。
A6总磷的测定
A6.1试剂
A6.1.1磷酸盐标准贮备液:
1mL溶液含有0.500mgPO-
称取0.7165克预先在100~105干燥至恒重的磷酸二氢钾(分析纯,准确至0.0002克,置于烧杯中,加水溶解,移入1000mL容量瓶中,用蒸馏水稀释至刻度,摇匀。
A6.1.2磷盐酸盐标准液:
1mL溶液含有0.020mgPO-
吸取20.00mL磷酸盐标准贮备液于500mL容量瓶中,用蒸馏水稀释至刻度,摇匀。
A6.1.3钼酸铵溶液:
称6克钼酸铵溶于约500mL水中,加入0.2克酒石酸锑钾和83mL浓硫酸,冷却后稀释至1升,混匀,贮于棕色瓶中,贮存期2个月。
A6.1.4抗坏血酸溶液:
称量17.6克抗坏血酸溶于约50mL水中,加入0.2克乙二胺四乙酸二钠和8mL甲酸,用水稀释至1升,混匀,贮于棕色瓶中,贮存期15天。
A6.1.5硫酸:
C1/2H2SQ=1mol溶液。
A6.1.6过硫酸铵:
24g/L溶液,贮存期7天。
A6.2仪器和设备
A6.2.1721分光光度计:
波长范围400~800nm
A6.2.2可调电炉:
800W
A6.3分析步骤
吸取10~25m冰样(如水样浑浊需预先过滤)^0mL锥形瓶中,加入1mL硫酸溶液和5mL过硫酸铵溶液,在可调电炉上加热至沸,保持20~30分钟(千万不要将水蒸干,但水样的体积也不要保留太多,大约^t~2mL即可,中间可往锥形瓶中补蒸馏水)取下,冷却至室温,移入50mL比色管(或容量瓶)内,加入5mL钼酸铵溶液,3mL抗坏血酸溶液,用水稀释至刻度,摇匀,于>5~30C下放置10分钟,在710nm处,用1cm的比色皿,以试剂空白为参比,测量其吸光度。
A6.4工作曲线的绘制
在一系列50mL容量瓶内分别加入0、1.002.003.004.005.006.00mL磷酸盐标准溶液,各加入水约20mL,然后加入5mL钼酸铵溶液和3mL抗坏血酸溶液,用水稀释至刻度,摇匀,于25~303下放置10分钟,在710nm处,用1cm的比色皿,以试剂空白为参比,测量其吸光度。
以PQ3-的mg数为横坐标,相对应的吸光度为纵坐标,绘制工作曲线。
总磷酸盐含量(以PO43-计mg/L)的计算如下:
C
PO43-(mg/L)=
V
式中:
C--测得的PQ3-的量,mg;
V--取水样的体积,mL
A7正磷酸盐含量的测定
吸取25mL水样(若PO-高时可适当少取)于50m比色管(或容量瓶)中,加入10mL水,再加入5mL!
目酸铵溶液,3mL抗坏血酸溶液,用水稀释至刻度,摇匀,于5~303下放置10分钟,用1cm的比色皿,在710nm处,以试剂空白为参比,测量其吸光度(用测总磷酸盐的工作曲线)。
正磷酸盐(以PO-计mg/L)的计算
C
正磷酸盐(以PQ3计mg/L)=-----1—00-
V
式中:
C—标准曲线上查得的PQ3-的量,mg;
V--取-水-样的体积,mL
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 水质 分析 常用 仪器 一览表
 冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《保险学概论》期末复习指导书蓝本答案要点.docx
《保险学概论》期末复习指导书蓝本答案要点.docx
