 5李千乐元素周期律与元素周期表.docx
5李千乐元素周期律与元素周期表.docx
- 文档编号:16241833
- 上传时间:2023-07-12
- 格式:DOCX
- 页数:27
- 大小:167.55KB
5李千乐元素周期律与元素周期表.docx
《5李千乐元素周期律与元素周期表.docx》由会员分享,可在线阅读,更多相关《5李千乐元素周期律与元素周期表.docx(27页珍藏版)》请在冰点文库上搜索。
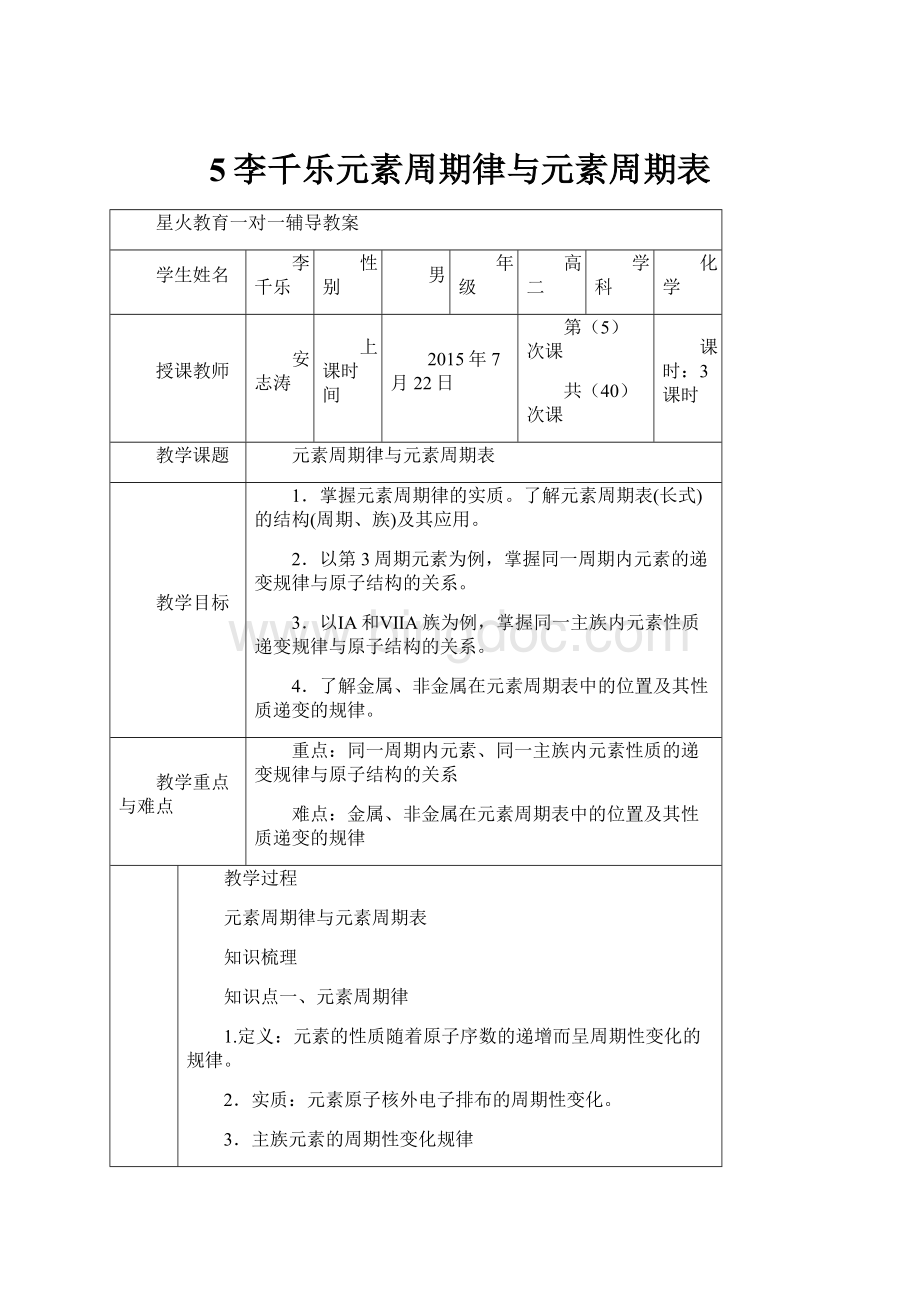
5李千乐元素周期律与元素周期表
星火教育一对一辅导教案
学生姓名
李千乐
性别
男
年级
高二
学科
化学
授课教师
安志涛
上课时间
2015年7月22日
第(5)次课
共(40)次课
课时:
3课时
教学课题
元素周期律与元素周期表
教学目标
1.掌握元素周期律的实质。
了解元素周期表(长式)的结构(周期、族)及其应用。
2.以第3周期元素为例,掌握同一周期内元素的递变规律与原子结构的关系。
3.以ⅠA和ⅦA族为例,掌握同一主族内元素性质递变规律与原子结构的关系。
4.了解金属、非金属在元素周期表中的位置及其性质递变的规律。
教学重点与难点
重点:
同一周期内元素、同一主族内元素性质的递变规律与原子结构的关系
难点:
金属、非金属在元素周期表中的位置及其性质递变的规律
教学过程
元素周期律与元素周期表
知识梳理
知识点一、元素周期律
1.定义:
元素的性质随着原子序数的递增而呈周期性变化的规律。
2.实质:
元素原子核外电子排布的周期性变化。
3.主族元素的周期性变化规律
内容
同周期(从左往右)
同主族(从上往下)
原子结构
电子层数
相同
依次增加
最外层电子数
依次增加1个
相同
原子半径
逐渐减小
逐渐增大
元素的性质
得电子能力
逐渐增强
逐渐减弱
失电子能力
逐渐减弱
逐渐增强
金属性
逐渐减弱
逐渐增强
非金属性
逐渐增强
逐渐减弱
主要化合价
最高正价:
+1→+7
最低负价:
主族序数-8
最高正价数=主族序数(O、F除外)
最高价氧化物对应水化物的酸碱性
酸性逐渐增强
碱性逐渐减弱
酸性逐渐减弱
碱性逐渐增强
非金属元素气态氢化物的形成及稳定性
气态氢化物的形成越来越易,其稳定性逐渐增强
气态氢化物的形成越来越难,其稳定性逐渐减弱
气态氢化物的还原性
逐渐减弱
逐渐增强
知识点二、元素周期表的结构
1.原子序数
按照元素在周期表中的顺序给元素编的序号。
原子序数=核电荷数=质子数=核外电子数。
2.编排原则
⑴按原子序数递增的顺序从左到右排列
⑵将电子层数相同的元素排列成一个横行.
⑶把最外层电子数相同的元素按电子层数递增的顺序从上到下排成纵行.
3.结构
(1)周期(7个横行,7个周期)
具有相同的电子层数的元素按照原子序数递增的顺序排列的一个横行称为一个周期。
(周期序数=电子层数)
短第1周期:
2种元素
周第2周期:
8种元素
期第3周期:
8种元素
⑵周期长第4周期:
18种元素
周第5周期:
18种元素
期第6周期:
32种元素
不完全周期:
第7周期:
26种元素
⑶注意:
①除第1、7周期外,每个周期都是从碱金属元素开始,逐渐过渡到卤素,最后以稀有气体元素结束.
②镧57La–镥71Lu共15种元素称镧系元素,位于第六周期.
它们的电子层结构和性质十分相似
③锕89Ac–铹103Lr共15种元素称锕系元素,位于第七周期.
它们的电子层结构和性质十分相似
④超铀元素:
92号元素铀以后的元素
4.族的分类
共十八纵行分为:
主族(A):
由短周期元素和长周期元素共同构成
副族(B):
完全由长周期元素构成
第Ⅷ族:
第8、9、10三个纵行为一个族
0族:
稀有气体元素,化学性质不活泼,化合价看成是0
知识点三、元素周期律和元素周期表的应用
1.元素的分区在元素周期表中,我们可以给金属元素和非金属元素分区。
周期
族
ⅠAⅡAⅢAⅣAⅤAⅥAⅦA
0
1
2
3
4
5
6
7
稀
有
气
体
2.位、构、性关系
(1)主族元素的最高正化合价与族序数、最外层电子数的关系:
最高正价=族序数=最外层电子数
(2)非金属元素的化合价与原子结构的关系
最高正价=最外层电子数
|负化合价数|=8-最外层电子数
3.元素周期表意义
(1)为发现新元素及预测其结构提供了线索。
(2)对其他与化学相关的科学技术有指导作用。
如:
可在金属和非金属的分界线处找到半导体材料;在元素周期表右上方处找到合成农药的元素;在过渡元素区寻找催化剂和耐高温、耐腐蚀的合金材料。
例1.下列关于元素周期表中周期的理解错误的是( )
A.周期表中每一个横行就是一个周期
B.每个周期的元素种类的数目不完全相同
C.周期的序数等于元素原子具有的电子层数
D.每个周期都是从碱金属开始到稀有气体结束
例2.下列各组元素性质的递变情况错误的是( )
A.Li、Be、B原子最外层电子数依次增多
B.P、S、Cl元素最高正价依次升高
C.N、O、F原子半径依次增大
D.Na、K、Rb的电子层数依次增多
例3.元素在周期表中的位置,反映了元素的原子结构和元素的性质。
下列说法正确的是( )
A.同一元素不可能既表现金属性,又表现非金属性
B.第三周期元素的最高正化合价等于它所处的主族序数
C.短周期元素形成离子后,最外层都达到8电子稳定结构
D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同
例4.下列有关原子结构和元素周期律的表述正确的是( )
①原子序数为15的元素的最高化合价为+3 ②ⅦA族元素是同周期中非金属性最强的元素 ③第二周期ⅣA族元素的原子核电荷数和中子数一定为6 ④原子序数为12的元素位于元素周期表的第三周期ⅡA族
A.①② B.①③ C.②④ D.③④
例5.元素的原子结构决定其性质和在周期表中的位置。
下列说法正确的是( )
A.元素原子的最外层电子数等于该元素的最高化合价
B.多电子原子中,在离核较近的区域内运动的电子能量较高
C.P、S、Cl得电子能力和最高价氧化物对应水化物的酸性均依次增强
D.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
例6.A、B、C为短周期元素,在周期表中所处的位置如右图所示。
A、C两元素的原子核外电子数之和等于B原子的质子数。
B原子核内质子数和中子数相等。
(1)写出A、B、C三种元素的名称__________、________、________。
(2)B位于元素周期表中第________周期,第________族。
(3)C的原子结构示意图为________,C的单质与H2反应的化学方程式为______________________________。
(4)比较B、C的原子半径:
B________C,写出A的气态氢化物与B的最高价氧化物对应的水化物反应的化学方程式______________________________。
知识点四、元素的金属性和非金属性强弱的比较
1.元素金属性强弱的比较
(1)根据金属单质与水(或酸)反应置换氢的难易程度:
Na、Mg、Al
Na>Mg>Al
(2)根据金属单质与盐溶液的置换反应:
Fe置换出Cu⇒Fe>Cu
(3)根据最高价氧化物对应水化物的碱性强弱:
碱性:
NaOH>Mg(OH)2>Al(OH)3⇒金属性:
Na>Mg>Al
2.元素非金属性强弱的比较
(1)根据非金属单质与H2化合的难易程度:
Cl2、Br2、I2
Cl>Br>I
(2)根据形成的氢化物的稳定性:
稳定性:
H2O>H2S⇒非金属性:
O>S
(3)根据非金属之间的相互置换:
Cl2置换出Br⇒Cl>Br
(4)根据最高价氧化物对应水化物的酸性强弱:
酸性:
H2SO4>H2CO3>H2SiO3⇒非金属性:
S>C>Si
例7下列有关叙述:
①非金属单质N能从M的化合物中置换出非金属单质M;②M原子比N原子容易得到电子;③两元素的阴离子在电极上放电时,N-优先于M-;④气态氢化物水溶液的酸性HmM>HnN;⑤氧化物对应水化物的酸性HmMOx>HnNOy;⑥单质熔点M>N。
能说明非金属元素M比N的非金属性强的是( )
A.②⑤⑥ B.②③
C.①②③⑥ D.①②③⑤
【变式训练1】下列事实不能说明金属元素甲的失电子能力一定比乙强的有( )
A.甲单质能从乙的盐溶液中置换出乙
B.甲、乙单质用导线连接后插入稀硫酸中,甲单质表面产生气泡
C.甲、乙两短周期元素原子的电子层数相同,甲的原子半径大于乙
D.甲、乙两元素的最高价氧化物对应水化物的碱性甲大于乙
知识点五、微粒半径大小的比较
1.同周期元素的微粒
同周期元素的原子或最高价阳离子或最低价阴离子半径随核电荷数增大而逐渐减小(稀有气体元素除外),如Na>Mg>Al>Si,Na+>Mg2+>Al3+,S2->Cl-。
2.同主族元素的微粒
同主族元素的原子或离子半径随核电荷数增大而逐渐增大,如Li 3.电子层结构相同的微粒 电子层结构相同(核外电子排布相同)的离子半径(包括阴、阳离子)随核电荷数的增加而减小。 如O2->F->Na+>Mg2+>Al3+(上一周期元素形成的阴离子与下一周期元素形成的阳离子有此规律)。 4.同种元素形成的微粒 同种元素原子形成的微粒电子数越多,半径越大。 如Fe3+ 5.电子数和核电荷数都不同的,可通过一种参照物进行比较 如比较A13+与S2-的半径大小,可找出与Al3+电子数相同,与S2-同族的元素O2-比较,Al3+ 例8短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。 下列说法正确的是( ) A.元素X与元素Z的最高正化合价之和的数值等于8 B.原子半径的大小顺序为: rX>rY>rZ>rW>rQ C.离子Y2-和Z3+的核外电子数和电子层数都不相同 D.元素W的最高价氧化物对应的水化物的酸性比Q的强 【变式训练2】已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( ) A.原子半径A>B>C>DB.原子序数a>b>c>d C.离子半径C3->D->B+>A2+D.单质的还原性A>B>D>C 知识点六、元素“位—构—性”的推断方法及技巧 (1)最外层电子数等于或大于3(小于8)的一定是主族元素。 (2)最外层有1个或2个电子,则可能是ⅠA、ⅡA族元素,还可能是副族元素或0族元素。 (3)最外层电子数比次外层电子数多的元素一定位于第2周期。 (4)根据原子序数确定元素在周期表中的位置 ①原子结构示意图法 按照原子核外电子排布规律画出原子结构示意图,然后由电子层数和最外层电子数确定其周期序数和族序数,如84号元素原子结构示意图为 ,该元素位于第6周期ⅥA族。 ②周期尾序推算法 首先熟记各周期0族元素原子序数,然后拿已知元素原子序数去比较。 若比某种稀有气体元素原子序数多1或2个,则该元素处于作比较的稀有气体元素的下周期ⅠA或ⅡA族。 若比某种稀有气体元素原子序数少5~1个,则该元素处于跟稀有气体元素同周期的ⅢA~ⅦA族。 例9J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素。 J R (1)M的离子结构示意图为________;元素T在周期表中位于第________族。 (2)J和氢组成的化合物分子有6个原子,其结构简式为________。 (3)M和T形成的化合物在潮湿的空气中冒白色烟雾,反应的化学方程式为________。 【变式训练3】 部分中学化学常见元素原子结构及性质如表所示: 序号 元素 结构及性质 ① A A单质是生活中常见金属,它有两种氯化物,相对分子质量相差35.5 ② B B原子最外层电子数是其内层电子总数的1/5 ③ C C是常见化肥的主要元素,单质常温下呈气态 ④ D D单质被誉为“信息革命的催化剂”,是常用的半导体材料 ⑤ E 通常情况下,E没有正化合价,A、B、C、D、F都能与E形成化合物 ⑥ F F在周期表中可以排在ⅠA族,也有人提出排在ⅦA族 ③ C C是常见化肥的主要元素,单质常温下呈气态 (1)A原子在周期表中的位置为________。 (2)B与C形成的化合物的化学式为________,它属于________化合物(填“离子”或“共价”)。 (3)①F与E可以形成原子个数之比分别为2: 1、1: 1的两种化合物X和Y,区别X与Y的水溶液的实验方法是 _________________________________________________; ②F与C组成的两种化合物M和N所含的电子数分别与X、Y相等,则M的分子构型为________,N的结构式为________。 (4)C与E都是较活泼的非金属元素,用化学方程式表明这两种单质的氧化性强弱________。 课堂练习 1.下列各组元素性质的递变情况错误的是( ) A.Li、Be、B原子最外层电子数依次增多 B.P、S、Cl元素最高正价依次升高 C.N、O、F原子半径依次增大 D.Na、K、Rb的电子层数依次增多 2.下列各图为元素周期表的一部分,表中的数字为原子序数,其中M元素原子序数为37的是( ) 3.应用元素周期律,判断下列语句,其中正确的组合是( ) ①碱金属单质的熔点随原子序数的增大而降低 ②砹(At)是ⅦA族元素,其氢化物的稳定性大于HCl ③硒(Se)的最高价氧化物对应水化物的酸性比硫酸弱 ④第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性 ⑤铊(Tl)与铝同主族,其单质既能与盐酸反应,又能与氢氧化钠溶液反应 ⑥第三周期金属元素的最高价氧化物对应水化物,其碱性随原子序数的增大而减弱 A.①③④B.①③⑥ C.③④⑤D.②④⑥ 4.短周期金属元素甲-戊在元素周期表中的相对位置如下表所示: 甲 乙 丙 丁 戊 下列判断正确的是( ) A.原子半径: 丙<丁<戊 B.金属性: 甲>丙 C.氢氧化物碱性: 丙>丁>戊 D.最外层电子数: 甲>乙 5.依据元素周期表及元素周期律,下列推断正确的是( ) A.H3BO3的酸性比H2CO3的强 B.Mg(OH)2的碱性比Be(OH)2的强 C.HCl、HBr、HI的热稳定性依次增强 D.若M+和R2-的核外电子层结构相同,则原子序数: R>M 6.A、B、C、D是原子序数均小于20的四种元素。 A与B同主族,且能形成BA3型分子。 B、C、D所形成的简单离子电子层结构相同,且B、C、D离子半径依次减小。 据此回答下列问题: (1)D元素在元素周期表中的位置是________; (2)将C单质的水溶液滴加到B与D所形成化合物的水溶液中,产生淡黄色沉淀,其反应的化学方程式为________________________________________; (3)实验室里除去BA2气体,可用下列试剂中的________(填字母); A.酸性高锰酸钾溶液B.浓H2SO4 C.NaOH溶液D.品红溶液 (4)由A、B、D三种元素所组成的某种盐的水溶液显碱性,其原因是(用离子方程式表示)_________________。 课后作业 1.下列叙述错误的是() ①热稳定性: H2O>HF>H2S ②熔点: Al>Na>K ③ⅡA族元素的阳离子与上周期稀有气体元素的原子具有相同的核外电子排布 ④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素 ⑤多电子原子中,在离核较近的区域内运动的电子能量较高 ⑥已知H2SO4(aq)+2NaOH(aq)=2H2O(l)+Na2SO4(aq)△H=-114.6kJ·mol-1则中和热为57.3kJ·mol-1 ⑦两个非金属元素原子间只可能形成共价键,而含金属元素的化合物中一定含离子键 A.②④⑥B.①⑤⑥C.②③④D.①⑤⑦ 2、Q、W、X、Y、Z是原子序数依次增大的短周期元素,X的焰色反应呈黄色。 Q元素的原子最外层电子数是其内层电子数的2倍。 W、Z最外层电子数相同,Z的核电荷数是W的2倍。 元素Y的合金是日常生活中使用最广泛的金属材料之一,下列说法正确的是() A.原子半径的大小顺序: rY>rX>rQ>rW B.X、Y的最高价氧化物的水化物之间不能发生反应 C.Z元素的氢化物稳定性大于W元素的氢化物稳定性 D.元素Q和Z能形成QZ2型的共价化合物 3.短周期元素T、Q、R、W在元素周期表中的位置如右图所示,其中T所处的周期序数与主族族序数相等。 它们的最高价氧化物的水化物依次为甲、乙、丙、丁。 下列叙述不正确的是() A.R的氧化物在空气中与其它物质作用可形成光化学烟雾 B.常温下丁的浓溶液可用T单质所制的容器来盛装 C.丁的浓溶液与Q的单质加热发生反应,可生成体积比为1: 2的两种气体 D.甲、乙、丙、丁受热均易分解 4.W、X、Y、Z是原子序数依次增大的四种短周期元素,已知: 四种元素的电子层数之和为10,且它们分别属于连续的四个主族;四种元素的原子中半径最大的是X原子。 下列说法正确的() A.四种元素中有两种元素在第二周期 B.W所在主族元素的原子次外层电子数可能为2或8,不可能为18 C.X、Y、Z的最高价氧化物对应的水化物两两之间能反应 D.工业上获得X、Y单质的方法主要是电解其熔融的氯化物 5.X.Y.Z.W均为短周期元素,它们在元素周期表中的位置如下图所示。 若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是() A.Z的氧化物对应的水化物一定是一种强酸 B.原子半径大小顺序是X>Y>Z C.Z单质与Fe反应形成的化合物中,铁元素显+3价 D.Y的单质比Z的单质更易与氢气反应 6.X、Y、Z、M、W为五种短周期元素。 它们在周期表的相对位置如下表: M X Y Z W 则下列说法正确的是: () A.Y、M形成的气态化合物在标准状况下的密度为0.76g.L-1 B.原子半径: W>Z>Y>X>M C.由X元素形成的单质一定是原子晶体 D.XZ2、X2M2、W2Z2均为直线型的共价化合物 7.X、Y、Z、W为四种短周期主族元素,它们在周期表中的位置如右图所示。 X的最高价氧化物和气态氢化物的分子都是由极性键形成的非极性分子。 下列性质比较中正确的是() A.最高价氧化物的水化物的酸性: Y W C.单质晶体的熔点由低到高的顺序: Y Z 8.X、Y、Z、R、W是原子序数依次增大的五种短周期元素。 Y和R同主族,可组成共价化合物RY2,Y和Z最外层电子数之和与W的最外层电子数相同。 25℃时,0.1mol/LX和W形成化合物的水溶液pH=1。 下列说法正确的是() A.Z与Y、Z与W形成的化合物的化学键完全相同 B.Y、Z、W三种元素组成的化合物的水溶液可能显碱性 C.简单离子的半径: Z﹥R﹥W﹥Y D.因非金属Y﹥R,所以X与Y组成化合物的沸点低于X与R组成的化合物 9.W、X、Y、Z是四种常见的短周期元素, 其原子半径随原子序数变化如下图所示。 已知W的一种原子的质量数为18,中子数 为10;X和Ne原子的核外电子数相差1; Y的单质是一种常见的半导体材料;Z是 同周期中非金属性最强的元素。 (1)Y位于元素周期表的位置,X与W元素形成的X2W2型化合物的电子式为 (2)Z的气态氢化物和溴化氢相比,较稳定的是(写化学式)。 (3)Y与Z形成的化合物硬度小、熔点低、沸点低,其晶体中存在的作用力有,其分子属于(填极性分子或非极性分子),它和足量水反应,有白色胶状沉淀产生,该反应的化学方程式是 (4)在25ºC、101kPa下,已知Y 的气态氢化物在氧气中完全燃烧后恢复至原状态,平均每转移1mol电子,放热190.0kJ,该反应的热化学方程式是 10.短周期主族元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其电子层数的1/2倍,Y是地壳中含量最高的金属元素,Z、W与Y同周期且互不相邻。 下列叙述正确的是() A.X与氧气反应可生成不止一种氧化物B.原子半径: W>Z>Y>X C.气态氢化物稳定性: HmZ>HnWD.W位于第3周期第ⅦA族 11、X、Y、Z、W、R五种短周期元素原子序数依次增大,X是周期表中原子半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,其氢氧化物能溶于强碱溶液但不溶于氨水,W单质是人类将太阳能转变为电能的常用材料。 下列说法正确的是( ) A.热稳定性: X2R>X2Y B.WY2能与碱反应,但不能与任何酸反应 C.Z位于第三周期第ⅢA族,Z与Y形成的化合物是一种比较好的耐火材料 D.使甲基橙变红色的溶液中: K+、R2-、ZY 、WY 一定能大量共存 12、短周期非金属元素甲~戊在元素周期表中的相对位置如右表所示,下面判断正确的是() A.原子半径: 甲<乙 甲 乙 丙 丁 戊 B.非金属性: 乙<丁 C.最高价氧化物的水化物的酸性: 丙<丁 D.最外层电子数: 丙>丁>戊 13、短周期元素W、X、Y、Z在元素周期表中的位置如右图所示。 其中Z的单质是一种重要半导体材料,广泛应用于电子工业的各个领域。 (1)W在元素周期表中的位置是。 (2)Z的原子结构示意图为。 (3)下列选项中,能证明元素非金属性X强于W的是。 A.原子序数: X>WB.最低化合价: X>W C.最简单氢化物的稳定性: X>WD.最高价氧化物的水化物酸性: X>W (4)元素周期表中与Z同周期的某金属元素形成的单质A,可发生如下图所示的转化: 其中化合物D是一种白色沉淀,则B中溶质的化学式为; C转化生成D的离子方程式为。 (5)表中Y的最高价氧化物对应水化物的化学式为Y(OH)n,在T℃时,其饱和溶液能使酚酞试液变红,原因是其溶液中的c(OH—)=mol·L—1(填计 算数值,已知: T℃,Ksp[Y(OH)n]=4.0×l0-12)。 14.A、B、C、D、E是原子序数依次增大的短周期主族元素。 A元素可形成多种同素异形体,其中一种是自然界最硬的物质;B的原子半径在短周期主族元素中最大;C原子核外电子占据7个不同的原子轨道;D的单质在常温常压下是淡黄色固体。 (1)E在元素周期表中的位置;B的基态原子核外电子排布式为。 (2)A、D、E中电负性最大的是(填元素符号);B、C两元素第一电离能较大的是(填元素符号)。 (3)A和D两元素非金属性较强的是(填元素符号),写出能证明该结论的一个事实依据。 (4)化合物AD2分子中共有个 键和个 键,AD2分子的空间构型是。 (5)C与E形成的化合物在常温下为白色固体,熔点为190℃,沸点为182.7℃,在177.8℃升华,推测此化合物为晶体。 工业上制取上述无水化合物方法如下: C的氧化物与A、E的单质在高温条件下反应,已知每消耗12kgA的
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 李千乐 元素周期律 元素 周期表
 冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《曹刿论战》知识点归纳与专项阅读.docx
《曹刿论战》知识点归纳与专项阅读.docx
