 最新中考化学典型专题抢分卷推断专题Word格式文档下载.docx
最新中考化学典型专题抢分卷推断专题Word格式文档下载.docx
- 文档编号:6415700
- 上传时间:2023-05-06
- 格式:DOCX
- 页数:19
- 大小:150.29KB
最新中考化学典型专题抢分卷推断专题Word格式文档下载.docx
《最新中考化学典型专题抢分卷推断专题Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《最新中考化学典型专题抢分卷推断专题Word格式文档下载.docx(19页珍藏版)》请在冰点文库上搜索。
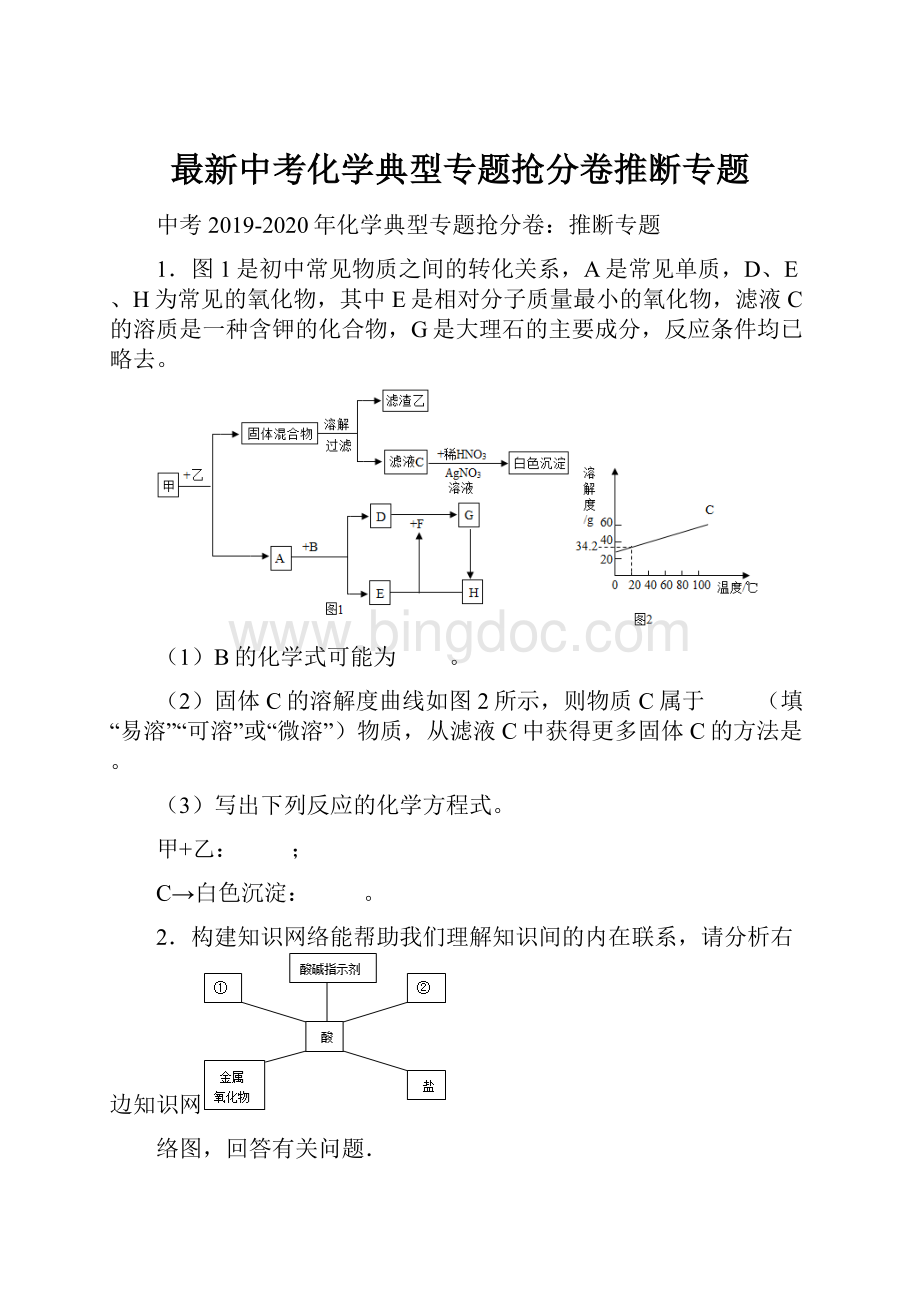
它们之间的部分转化关系如图所示(图中反应条件及部分反应物、生成物已省略)
回答下列问题:
(1)写出下列物质的化学式:
A ;
D 。
(2)写出由物质C转化为物质B的化学方程式 ,写出该反应的基本反应类型 。
(3)写出物质C与过氧化钠(Na2O2)反应生成碳酸钠和物质A的化学方程式
。
7.甲、乙、丙、X是初中化学常见的四中物质。
它们的转化关系如图所示(部分产物略去,图中“→”表示甲和丙都能与X反应生成乙)。
(1)若甲为二氧化碳,乙为一氧化碳,丙为氧气。
①X的化学式为 。
②甲、乙、丙三种气体中有毒的是 。
(2)若甲为碳酸氢钠,乙为氯化钠,丙为碱。
①丙的名称为 。
②物质X (“能”或“不能”)清除铁制品表面的锈。
(3)若X为石灰水,甲为碳酸钠,丙为气体。
①X与甲的溶液反应,其反应的类型是 。
②丙与足量X反应的化学方程式为 。
8.A、B、C、D、E、F都是初中化学中常见的化合物,其中A、B是盐,且B中含有钠元素;
D是酸,C为白色沉淀。
它们相互之间在溶液中可发生如下反应:
①C+D=A+2F②2E+D=B+2F③A+2E=C↓+B
根据上述信息回答问题:
(1)写出物质的化学式:
D ,F ;
(2)写出下列反应的化学方程式:
反应① ;
反应③ 。
9.A、B、C、D、E、F六种物质是初中化学中的常见物质,有如图所示的转化关系。
已知A在反应前后质量和化学性质都没有发生改变,D和E均为单质,E在D中燃烧产生大量白烟。
(1)A在此反应中其 作用;
(2)F的化学式为 ;
(3)写出①的化学反应方程式 ;
(4)说出物质C的一点用途 。
10.A、B、C、D、E是初中常见的五种物质,其中E是黑色固体,且与B在一定条件下反应有红色物质生成,C的固体俗称干冰。
①、②、③、④的反应类型分别是复分解反应、化合反应、分解反应和置换反应。
图中“﹣”表示两端物质间能发生反应,“→”表示物质间的转化关系,部分反应物、生成物及反应条件已略去。
请回答下列问题:
D ,C 。
(2)写出B与E反应的化学方程式:
11.下列框图中的物质均为初中化学常见的物质,其中A是建筑材料的主要成分,B属于氧化物,如图是它们之间的相互转化关系。
请回答:
A. E. 。
(2)得到F溶液的操作Ⅰ的名称为:
(3)写出B→G的化学方程式 。
(4)若K是蓝色沉淀,反应②的化学方程式为 。
12.A→D是初中化学常见的不同类别的物质,已知化合物A、B中含有两种相同的元素。
它们之间的关系如图所示,“一”表示两种物质之间可以相互反应,“→”表示一种物质可生成另一种物质。
分析推理,回答:
(1)写出“C一B”、A与D反应且有浅绿色溶液生成的化学方程式。
(2)说出物质A的一种具体用途。
13.A、B、C为初中化学常见的物质,它们之间存在如图所示的转化关系(在一定条件下均能一步实现)。
(1)若A、C组成元素相同,C是一种最常用的溶剂,则B→C的化学方程式为 。
(2)若B、C组成元素相同,A为黑色固体单质,B为可燃性气体化合物,则C的化学式为 。
(3)若A、B、C分别为CO2、Na2CO3溶液、CaCO3三种物质中的一种,B→C的反应为复分解反应,则B→C的化学方程式为 ,该反应能发生的原因是 。
14.图中A﹣J是初中化学常见物质,且分别由H、O、Al、S、Cl、Fe、Cu中的一种或几种元素组成。
A、D、E、G、I均为单质,A在空气中表面生成一层致密的氧化膜,具有很好的抗腐蚀性能,E为紫红色固体;
J为金属氧化物;
B、C均由三种元素组成。
图中“﹣”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系;
部分反应物、生成物或反应物条件已略去。
(1)写出E的化学式:
(2)写出A与B反应的化学方程式 。
(3)E和I反应的基本反应类型为 。
(4)写出G→F反应的化学方程式 。
15.已知A、B、C、D、E是初中化学中常见的不同类别的物质,它们之间的关系如图所示(“→”表示物质间的转化关系,“﹣”表示两端的物质能发生化学反应).A是使用最广泛的金属,C是常用的食品干燥剂,E是配制波尔多液的主要成份之一,其溶液为蓝色,F是由三种元素组成的化合物,请回答下列问题:
(1)写出化学式:
B ;
E .
(2)物质C所属的物质类别是 ,选择C作为食品干燥剂的原因有
(答两条即可)
(3)写出D转化为F的化学方程式 .
(4)B在生产上的用途有 ,上述反应没有包含的基本反应类型是 .
16.A、B、C、D、E是初中化学中的五种常见物质.C、D是单质,C为紫红色固体,D被认为是最清洁的能源.B的浓溶液常用做干燥剂.已知Fe和A、B的水溶液分别能发生反应:
①Fe+A→C+E;
②Fe+B→D+E.
(1)写出A、B、C的化学式:
A ,B ,C .
(2)现有Fe和A、C三种固体组成的混合物,小刚想测定该混合物中C物质的质量分数,他设计并完成了以下实验:
你认为,小刚的实验数据处理是否正确(填“正确”或“不正确”) ,理由是 .
17.如图中的六个原A、B、C、D、E、F分别表示六种物质,蓝色溶液A与C反应能生成两种沉淀,B为氧化物,D、E、F分别是碳酸钠溶液、稀硫酸和氢氧化钠溶液中的一种,E中溶质可用于生产洗涤剂,用“→”表示一种物质能转化为另一种物质,用两个圆相切或“﹣﹣”表示两种物质可以发生化学反应,六种物质之间的部分反应及转化关系如图所示.请利用初中化学知识回答下列问题:
(1)写出A、E的化学式 、 ;
(2)C与F反应的化学方程式为 ;
(3)试写出一个有B生成的置换反应的化学方程式 .
参考答案
1.【答案】
(1):
CH4或C2H5OH(合理即可)
(2)易溶;
蒸发结晶;
(3)2KClO3
2KCl+3O2↑;
KCl+AgNO3=KNO3+AgCl↓。
2.【答案】
(1)①活泼金属;
H2;
(2)Fe2O3+6HCl═2FeCl3+3H2O;
(3)Ca(OH)2+CuSO4═Cu(OH)2↓+CaSO4.
3.【答案】本题属于物质的推断题,为了确定物质的组成,本题可以通过的实验流程中不同的现象,从而得出实验结论.本题的突破点是:
因为“A、B为两种黑色粉末”,“A为单质,D为红色单质”,则推测D为铜,因此B是氧化铜,A为碳,结合图框,可知C为二氧化碳.根据“E是常用的建筑材料”,则推出为碳酸钙.带入检验,符合题意.
根据分析,则B的化学式为CuO;
反应①为氧化铜与碳反应生成铜和二氧化碳,所属的基本反应类型为置换反应;
反应③为碳酸钙高温生成二氧化碳和氧化钙或碳酸钙与稀盐酸反应生成二氧化碳,其化学方程式为CaCO3
CO2↑+CaO或CaCO3+2HCl═CaCl2+H2O+CO2↑.
故答案为:
CuO;
置换反应;
CaCO3
4.【答案】
(1)二氧化碳(合理即可);
(2)Ca(OH)2+2HCl═CaCl2+2H2O;
CO2+Ca(OH)2═CaCO3↓+H2O(合理即可);
(3)SO2+2KOH═K2SO3+H2O.
5.【答案】
(1)③④;
(3)NaOH+HCl═NaCl+H2O;
(4)CO2+H2O+Na2CO3═2NaHCO3。
6.【答案】A、B、C、D是初中化学常见的物质,D是大理石的主要成分,所以D是碳酸钙,B、C为氧化物,且B为有毒气体,所以B是一氧化碳,一氧化碳和C可以相互转化,碳酸钙和C也可以相互转化,所以C是二氧化碳,A为无色气体单质,会转化成一氧化碳和二氧化碳,所以A是氧气,经过验证,推导正确;
(1)A是O2,D是CaCO3;
故填:
O2;
CaCO3;
(2)C转化为物质B是二氧化碳和碳高温生成一氧化碳,化学方程式为:
CO2+C
2CO;
该反应是两种物质生成一种物质的反应,属于化合反应,故填:
化合反应;
(3)物质C与过氧化钠(Na2O2)反应生成碳酸钠和物质A,是二氧化碳和过氧化钠反应产生碳酸钠和氧气,故反应的方程式为:
2CO2+2Na2O2═2Na2CO3+O2。
7.【答案】
(1)①C;
②一氧化碳(或乙或CO);
(2)①氢氧化钠;
②能;
(3)①复分解反应;
②CO2+Ca(OH)2=CaCO3↓+H2O;
8.【答案】
(1)H2SO4,H2O;
(2)Mg(OH)2+H2SO4=MgSO4+2H2O;
MgSO4+2NaOH=Mg(OH)2↓+Na2SO4。
9.【答案】
(1)催化;
(2)P2O5;
(3)2H2O2
2H2O+O2↑;
(4)配制溶液等。
10.【答案】
(1)碳酸钠和盐酸反应生成氯化钠和水和二氧化碳,碳酸钠和氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠,碳酸钙在高温的条件下生成氧化钙和二氧化碳,因此A是碳酸钠,D是碳酸钙;
C的固体俗称干冰,因此C是二氧化碳;
CO2;
(合理即可)
(2)黑色固体碳和黑色固体氧化铜在高温的条件下生成红色固体铜和二氧化碳,配平即可;
C+2CuO
2Cu+CO2↑;
11.【答案】
(1)CaCO3;
Ca(OH)2;
(2)过滤;
(3)CuO+H2SO4=CuSO4+H2O;
(4)CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
12.【答案】
(1)C和B、A与D反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O;
Fe+H2SO4=FeSO4+H2↑;
(2)A物质可以用来除锈;
13.【答案】
(1)若A、C组成元素相同,C是一种最常用的溶剂,过氧化氢分解会生成水和氧气,氢气在氧气中点燃生成水,所以A是过氧化氢溶液、B是氧气、C是水;
2H2+O2
2H2O;
(2)若B、C组成元素相同,A为黑色固体单质,B为可燃性气体化合物,则A是碳,B是一氧化碳,一氧化碳和氧气点燃生成二氧化碳,所以C是二氧化碳;
(3)若A、B、C分别为CO2、Na2CO3溶液、CaCO3三种物质中的一种,B→C的反应为复分解反应,则B为Na2CO3溶液,与Ca(OH)2[或CaCl2、Ca(NO3)2]反应可生成C物质CaCO3,该反应能够发生的原因是:
符合复分解反应的条件,反应物均可溶,生成物有沉淀;
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH(合理即可);
14.【答案】
(1)Cu;
(2)2Al+3CuSO4=3Cu+Al2(SO4)3;
(3)化合反应;
(4)H2+Cl2
2HCl。
15.【答案】
(1)根据题目给出的流程图和信息:
A是使用最广泛的金属,C是常用的食品干燥剂,E是配制波尔多液的主要成份之一,其溶液为蓝色,因此A是铁,C是氧化钙,E是硫酸铜;
氧化铜与硫酸反应生成硫酸铜和水,因此B是硫酸;
H2SO4;
CuSO4;
(2)C是氧化钙,属于氧化物或金属氧化物;
选择C氧化钙为食品干燥剂的原因有:
安全无毒,价格低廉等;
氧化物;
安全无毒,价格低廉;
(答案合理即可)
(3)F是由三种元素组成的化合物,氢氧化钙和碳酸钠反应生成碳酸钙白色沉淀和氢氧化钠,配平即可;
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(4)硫酸在生产上的用途有:
金属除锈、制氢气等;
上述反应没有包含的基本反应类型是分解反应;
金属除锈;
分解反应;
16.【答案】
(1)由“C、D是单质,C为紫红色固体”可以推断,C为Cu;
最清洁的能源是H2,故可推断D是H2;
由“B的浓溶液常用做干燥剂”可判断B是浓硫酸;
故②Fe+B→D+E的化学方程式为:
Fe+H2SO4=FeSO4+H2↑,故可推断,E为FeSO4;
那么①Fe+A→C+E的化学方程式为:
Fe+CuSO4=FeSO4+Cu;
故可推断A为CuSO4.
故选CuSO4、H2SO4、Cu.
(2)不正确.4.2g紫红色固体中包含有铁和硫酸铜反应生成的铜(铁和硫酸铜反应生成了铜或4.2g紫红色固体,不只是原来的C物质,或4.2g紫红色固体的质量大于原来C物质的质量.其它合理答案均可.没有文字说明不给分).
17.【答案】
(1)CuSO4、Na2CO3;
(2)Ba(OH)2+H2SO4═BaSO4↓+2H2O;
(3)H2+CuO
Cu+H2O.
二、中考化学推断题
2.已知:
A、B、C、D、E、F、G等物质均由前18号元素组成,其相互间的转化关系如图所示;
A是生活中的常见液态物质;
D是一种单质,其构成原子X的最外层电子数是次外层电子数的2倍;
E是一种碱,其阳离子存在于一种常见生活调味剂中。
(1)相同条件下,B的密度___(填“大与”或“小于”或“等于”)空气密度;
(2)鉴别F的方法是____;
(3)请画出构成D单质的X的原子结构示意图___;
(4)酸碱都有腐蚀性。
如果不慎将E沾到皮肤上,其正确处理方法是___;
(5)写出G与氢氧化钙反应的化学方程式___。
【答案】小于将气体通入澄清石灰水,石灰水变浑浊,证明该气体是二氧化碳
先用大量的水冲洗,然后涂上硼酸Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
【解析】
【分析】
A是生活中的常见液态物质,A通电会生成B、C,所以A是H2O,B、C是氢气或氧气中的一种,D是一种单质,其构成原子X的最外层电子数是次外层电子数的2倍,所以D是木炭,木炭可以在C中充分燃烧,所以C是O2,B就是H2,木炭和氧气反应生成二氧化碳,所以F是CO2,E是一种碱,其阳离子存在于一种常见生活调味剂中,所以E是NaOH,NaOH和二氧化碳反应生成碳酸钠和水,所以G是Na2CO3,经过验证,推导正确。
【详解】
(1)B是氢气,其密度小于空气密度;
(2)F是二氧化碳,鉴别二氧化碳的方法是:
将气体通入澄清石灰水中,石灰水变浑浊,证明该气体是二氧化碳;
(3)X是木炭,碳的原子结构示意图是:
;
如果不慎将氢氧化钠沾到皮肤上,正确处理方法是:
先用大量的水冲洗,然后涂上硼酸溶液;
(5)通过推导可知G是Na2CO3,Na2CO3和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:
Na2CO3+Ca(OH)2═CaCO3↓+2NaOH。
【点睛】
在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可。
水是生活中的常见液态物质,氢氧化钠是一种碱,其阳离子存在于一种常见生活调味剂中是该题的突破口。
3.A→I是初中化学常见的物质,它们的相互转化关系如图所示,其中A、B组成元素相同且常温下为液体,C、D、E为无色气体,E为温室气体之一,H是石灰石的主要成分。
D_____;
F_____。
(2)写出反应①的化学方程式_____,基本反应类型为_____。
(3)写出反应②的化学方程式_____。
【答案】H2C2H2O2
2H2O+O2↑分解反应Ca(OH)2+CO2═CaCO3↓+H2O
根据题目给出的流程图和信息:
根据“H是石灰石的主要成分”,则推测H为碳酸钙;
结合图框:
B通电生成D、C,则B为水,D为氢气,C为氧气;
A分解生成C、F,则为双氧水分解生成氧气和水;
根据二氧化碳与氢氧化钙反应生成碳酸钙和水等知识,则F为碳,E为二氧化碳,G为氢氧化钙,代入检验,符合题意。
(1)D氢气,化学式为H2;
F为碳,化学式为C;
(2)反应①为双氧水分解生成氧气和水,反应的化学方程式:
2H2O2
2H2O+O2↑;
其反应的基本反应类型为分解反应;
(3)反应②为二氧化碳与氢氧化钙反应生成碳酸钙和水,其反应的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O。
首先根据将题中有特征的物质推出,找出突破口,然后结合题中的反应和转化图推出其他的物质即可。
4.A、B、C、D、E、F、G七种物质都是日常生活和生产中常见的物质,各物质间存在如下转化关系(反应的条件已省略):
已知:
B、C两种物质在不同情况下可分别发生①和②两个反应;
A﹣G七种物质都是由非金属元素组成的,其中只有一种物质是盐,一种物质是单质;
且B的相对分子质量大于C。
(1)请写出下列物质的化学式:
A_____;
G_____;
(2)请写出E+F→B+C的化学方程式:
_____。
【答案】NH4HCO3H2CO3C6H12O6+6O2
6CO2+6H2O
A、B、C、D、E、F、G七种物质都是日常生活和生产中常见的物质,七种物质都是由非金属元素组成的,其中只有一种物质是盐,则该种物质一定为铵盐,假设为碳酸铵,碳酸铵加热分解生成氨气、水和二氧化碳;
二氧化碳和水反应生成碳酸,在一定条件可生成葡萄糖;
碳酸分解又生成二氧化碳和水,葡萄糖和氧气在一定条件下生成二氧化碳和水,代入验证符合转化关系;
(1)所以A为碳酸氢铵,B为二氧化碳,C为水,D为氨气,G为碳酸;
(2)E+F→B+C的反应是葡萄糖和氧气在一定条件下生成二氧化碳和水,化学方程式为:
C6H12O6+602
6CO2+6H2O。
5.图示中A~F是初中化学常见的物质,其中A是一种钠盐,C、D为氧化物,A、B、C、D、E中都含有氧元素,且物质C的固体俗称“干冰”。
图中“—”表示相连的两种物质之间可以发生反应,“→”表示物质间存在着相应的转化关系(部分反应物、生成物及反应条件已略去)。
请分析后作答:
(1)物质C的化学式__________。
(2)反应①的基本反应类型是______________。
(3)反应②的化学方程式_______________________。
(4)写出B的一种用途_________________
【答案】CO2复分解反应BaCl2+H2SO4=2HCl+BaSO4↓补钙剂(合理即可)
A是一种钠盐,C、D为氧化物,A、B、C、D、E中都含有氧元素,且物质C的固体俗称“干冰”,因此C是二氧化碳;
碳酸钠和硫酸反应生成硫酸钠和水和二氧化碳,碳酸钠和氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠,碳酸钙在高温的条件下生成氧化钙和二氧化碳,硫酸和氯化钡反应生成硫酸钡和盐酸,因此A是碳酸钠,B是碳酸钙,D是氧化钙,E是硫酸,F是盐酸。
(1)物质C的固体俗称“干冰”,因此C是二氧化碳;
化学式为:
(2)D是氧化钙,F是盐酸,反应①是氧化钙和盐酸反应生成氯化钙和水,属于复分解反应;
(3)E是硫酸,F是盐酸,反应②是硫酸和氯化钡反应生成硫酸钡和盐酸,反应方程式为:
BaCl2+H2SO4=BaSO4↓+2HCl。
(4)B是碳酸钙,可作补钙剂(合理即可)。
6.现有铁、氧化铁、稀盐酸、氢氧化钠、碳酸钠等五种物质,它们之间存在如图所示相互反应和转化关系(“﹣”表示相连的物质间能反应,“→”表示物质间的转化).回答下列问题
(1)C的化学式是_____,C与Fe反应的化学方程式是_____。
(2)要实现A转化为B,需要的另一种反应物是_____,B与C反应的基本反应类型是_____。
(3)D转化为铁的化学方程式是_____。
【答案】HClFe+2HCl═FeCl2+H2↑二氧化碳复分解反应Fe2O3+3CO
2Fe+3CO2
根据“现有铁、氧化铁、稀盐酸、氢氧化钠、碳酸钠等五种物质”,结合图,能与其它四种物质反应的物质为稀盐酸,而氧化铁可以转化为铁,氢氧化钠可以转化为碳酸钠,故推测A为氢氧化钠,B为碳酸钠,D为氧化铁,代入检验。
(1)根据分析,C的化学式是HCl,C与Fe反应的化学方程式是Fe+2HCl═FeCl2+H2↑。
(2)要实现A转化为B,即氢氧化钠转化碳酸钠,需要的另一种反应物是二氧化碳;
B与C反应,即碳酸钠与稀盐酸生成氯化钠和二氧化碳、水,反应的基本反应类型是复分解反应。
(3)D转化为铁,即氧化铁与一氧化碳反应生成铁,故反应的化学方程式是Fe2O3+3CO
2Fe+3CO2。
(1)HCl,Fe+2HCl═FeCl2+H2↑.
(2)二氧化碳,复分解反应。
(3)Fe2O3+3CO
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 最新 中考 化学 典型 专题 分卷 推断
 冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《安全在我心中生命在我手中》主题班会教案.docx
《安全在我心中生命在我手中》主题班会教案.docx
