 高中化学选修4 第3章 水溶液中的离子平衡 解析Word下载.docx
高中化学选修4 第3章 水溶液中的离子平衡 解析Word下载.docx
- 文档编号:8393435
- 上传时间:2023-05-11
- 格式:DOCX
- 页数:50
- 大小:221.10KB
高中化学选修4 第3章 水溶液中的离子平衡 解析Word下载.docx
《高中化学选修4 第3章 水溶液中的离子平衡 解析Word下载.docx》由会员分享,可在线阅读,更多相关《高中化学选修4 第3章 水溶液中的离子平衡 解析Word下载.docx(50页珍藏版)》请在冰点文库上搜索。
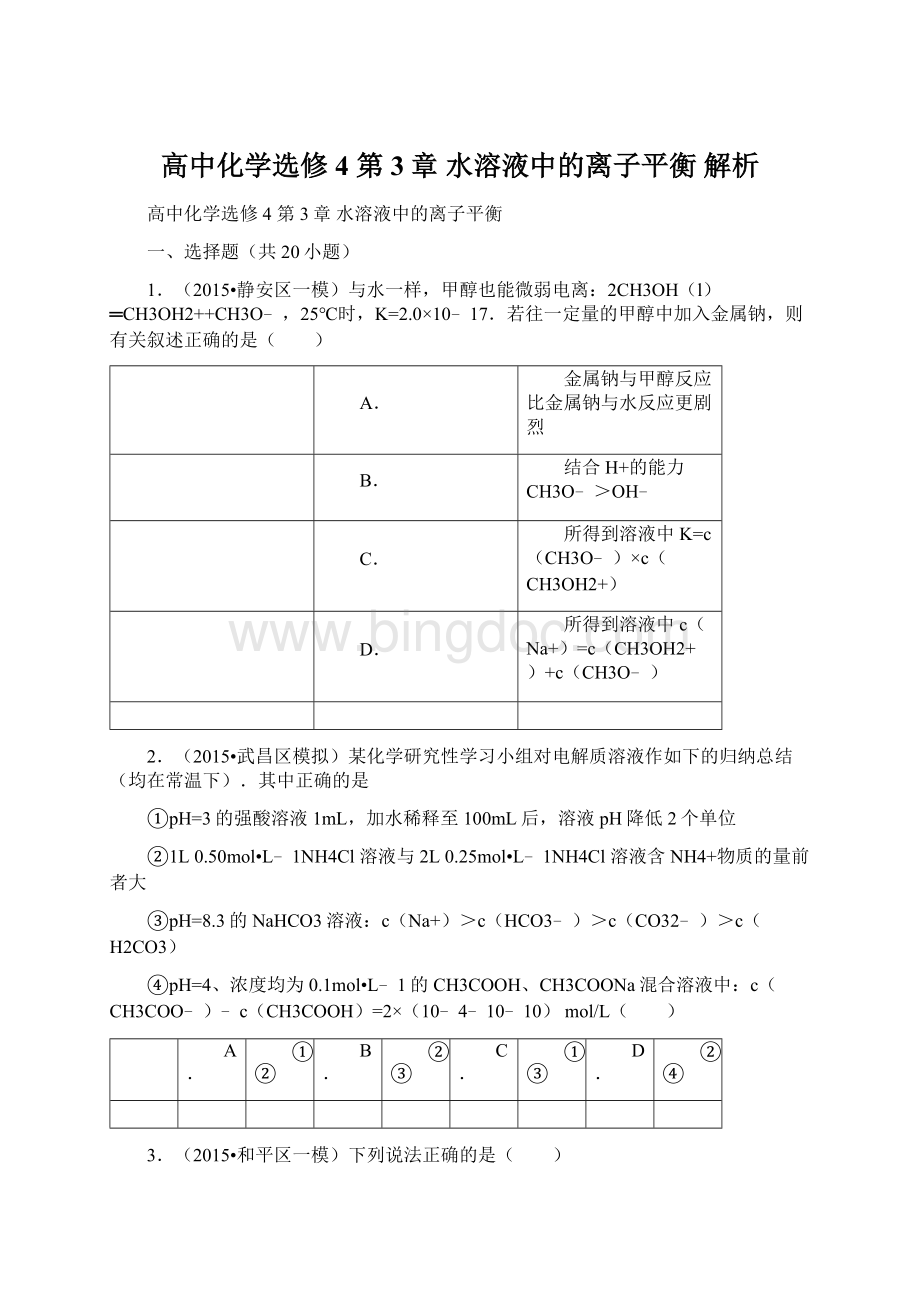
②④
3.(2015•和平区一模)下列说法正确的是( )
常温下将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4
未确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH.若pH>7,则H2A是弱酸;
pH<7,H2A是强酸
已知酸性HF>CH3COOH,物质的量浓度相等的NaF与CH3COOK溶液中:
[c(Na+)﹣c(F﹣)]<[c(K+)﹣c(CH3COO﹣)]
相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水②0.1mol/L盐酸③0.1mol/L氯化镁溶液④0.1mol/L硝酸银溶液中,Ag+浓度:
①>④=②>③
4.(2015•天津校级模拟)部分弱酸的电离平衡常数如下表:
( )
弱酸
HCOOH
HCN
H2CO3
电离平衡常数(25℃)
K=1.777×
10﹣4
K=4.9×
10﹣10
K1=4.3×
10﹣7
K2=5.6×
10﹣11
0.1mol•L﹣1NaHCO3溶液中浓度的大小:
c(Na+)>c(HCO3﹣)>c(H+)>c(OH﹣)
少量的CO2通入到NaCN溶液中:
2CN﹣+H2O+CO2=2HCN+CO32﹣
用0.1mol•L﹣1NaOH溶液中和等浓度等体积的HCN和HCOOH时所需NaOH溶液体积相等
相同体积的0.1mol•L﹣1HCOONa溶液比0.1mol•L﹣1NaCN溶液所含离子总数相等
5.(2014•安徽模拟)下列图象不符合事实是( )
图①:
pH相同的H2S溶液、稀H2SO4溶液、H2SO3溶液露置于空气中一段时间后,溶液的pH随时间的变化情况
图②:
表示向乙酸溶液中通入NH3过程中溶液导电性的变化
图③:
将铜粉加入到一定量浓硝酸中产生的气体与加入铜量的变化情况
图④知合成甲醇的热化学方程式为CO(g)+2H2(g)=CH3OH(g)△H=﹣(b﹣a)kJ•mol﹣1
6.在体积都为1L、pH都等于2的盐酸和醋酸溶液中,分别投入等量的锌粒,则下图所示比较符合客观事实的是( )
7.(2015•闸北区一模)25℃时,已知弱酸的电离常数:
Ki(CH3COOH)=1.8×
10﹣5;
Ki1(H2CO3)=4.4×
10﹣7;
Ki2(H2CO3)=4.7×
10﹣11;
Ki(HClO)=4.0×
10﹣8.则下列说法正确的是( )
物质的量浓度相等的溶液pH关系:
pH(NaClO)>pH(Na2CO3)>pH(CH3COONa)
向NaClO溶液中通少量CO2:
CO2+NaClO+H2O→NaHCO3+HClO
amol/LHClO与bmol/LNaOH溶液等体积混合后所得溶液中c(Na+)>c(ClO﹣),则a一定小于b
向氯水中加入NaHCO3固体,可以增大氯水中次氯酸的浓度
8.(2015•肇庆二模)常温下,下列表述正确的是( )
pH=3的CH3COOH溶液的浓度小于pH=2的盐酸的浓度
向NaHCO3溶液中加入少量NaOH固体,可抑制HCO3﹣的水解,使c(HCO3﹣)增大
将任意量的CH3COOH溶液与NaOH溶液混合,其混合溶液均存在:
c(Na+)+c(H+)=c(CH3COO﹣)+c(OH﹣)
Na2CO3溶液中:
c(Na+)>c(CO32﹣)>c(OH﹣)=c(HCO3﹣)>c(H+)
9.(2015•云南模拟)下列对图象描述正确的是( )
图表示体积和pH值均相同的稀硫酸和醋酸,与足量的镁反应生成H2量的关系
图表示向NaOH溶液中滴加稀盐酸,溶液导电性变化的关系
图表示2SO2(g)+O2(g)⇌2SO3(g)反应过程中,SO2和O2反应速率大小关系
图表示向氨水中滴加稀硫酸时,溶液的pH大小变化关系
10.常温下某H2CO3溶液的pH约为5.5,c(CO32﹣)约为5×
10﹣11mol/L,该溶液中浓度最低的离子是( )
HCO3﹣
CO32﹣
H+
OH﹣
11.(2015•岳阳模拟)25℃时,几种弱酸的电离常数如下:
25℃时,下列说法正确的是( )
弱酸的化学式
CH3COOH
H2S
电离常数(25℃)
1.8×
10﹣5
4.9×
K1=1.3×
K2=7.1×
10﹣15
等物质的量浓度的各溶液pH关系为:
pH(CH3COONa)>pH(Na2S)>pH(NaCN)
amol/LHCN溶液与bmol/LNaOH溶液等体积混合,所得溶液中c(Na+)>c(CN﹣),则a一定小于或等于b
NaHS和Na2S的混合溶液中,一定存在c(Na+)+c(H+)=c(OH﹣)+c(HS﹣)+2c(S2﹣)
某浓度的NaCN溶液的pH=d,则其中由水电离出的c(OH﹣)=10﹣dmol/L
12.(2015•乌鲁木齐模拟)部分弱酸的电离平衡常数如表,表述肯定正确的是( )
H2SO3
HClO
电离平衡常数
(25℃)
K1=4.30×
K1=1.54×
10﹣2
K=2.95×
10﹣8
K2=5.61×
K2=1.02×
相同温度时三种溶液的pH关系:
Na2CO3>NaClO>Na2SO3
ClO﹣+H2O+CO2→HClO+HCO3﹣
2ClO﹣+SO2+H2O→2HClO+SO32﹣
等体积、等物质的量浓度的HClO和Na2CO3混合后溶液呈碱性
13.(2015•宝山区一模)某种碳酸饮料中主要含柠檬酸、碳酸、白砂糖、苯甲酸钠等成分,常温下测得其pH约为3.5,下列说法不正确的是( )
柠檬酸的电离会抑制碳酸的电离
该碳酸饮料中水的电离受到抑制
常温下,该碳酸饮料中KW的值大于纯水中KW的值
打开瓶盖冒出大量气泡,是因为压强减小,降低了CO2的溶解度
14.(2015•南昌校级二模)某温度下,已知CH3COOH、HClO、H2CO3、H3PO4电离平衡常数如下表所示,则0.1mol•L﹣1的下列各溶液pH最大的是( )
表:
几种弱酸的电离平衡常数
酸
电离常数
Ka=1.8×
Ka=3.0×
Ka1=4.3×
10﹣7,Ka2=5.6×
H3PO4
Ka1=7.5×
10﹣3,Ka2=6.2×
10﹣8,Ka3=2.2×
10﹣13
CH3COONa
NaClO
Na2CO3
Na3PO4
15.(2015•朝阳区校级三模)已知:
HCl为强酸,下列对比实验不能用于证明CH3COOH为弱酸的是( )
对比等浓度的两种酸的pH
对比等浓度的两种酸,与相同大小镁条反应的初始速率
对比等浓度、等体积的两种酸,与等量NaOH溶液反应后放出的热量
对比等浓度、等体积的两种酸,与足量Zn反应,生成H2的体积
16.(2015•龙岩模拟)常温下,0.2mol•L﹣1的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法不正确的是( )
HA为弱酸
该混合液pH>7
图中X表示HA,Y表示OH﹣,Z表示H+
该混合溶液中:
c(A﹣)+c(Y)=c(Na+)
17.(2015•韶关一模)对常温下0.1mo1/L的醋酸溶液,以下说法正确的是( )
由水电离出来的c(H+)=1.0×
10﹣13mo1/L
c(CH3COOH)>c(H+)>c(CH3COO﹣)>c(OH﹣)
与同浓度的盐酸分别加水稀释10倍:
pH(醋酸)>pH(盐酸)
与等浓度等体积NaOH溶液反应后的溶液中:
c(CH3COOH)+c(CH3COO﹣)=0.1mo1/L
18.(2015•宁城县一模)下列说法正确的是( )
常温下pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度前者比后者大
用饱和Na2CO3溶液处理BaSO4沉淀,可将BaSO4转化为BaCO3
BaSO4(s)+4C(s)═BaS(s)+4CO(g)室温下不能自发进行,说明该反应的△H<0
为准确测定盐酸与氢氧化钠溶液反应的中和热,所用酸和碱的物质的量应相等
19.(2016•枣庄校级二模)已知H2CO3的电离平衡常数Ka1=4.4×
10﹣7,Ka2=4.7×
10﹣11.向0.1mol/LNaOH溶液中通入CO2,若溶液的pH=10(不考虑溶液的体积变化),则下列说法正确的是( )
2c(CO32﹣)+c(HCO3﹣)=0.1mol/L
=0.47
该溶液中加BaCl2溶液,溶液pH增大
在溶液中加水,使体积扩大到原来的10倍,则溶液pH明显变小
20.(2015•河东区一模)下表是在相同温度下三种酸的一些数据,下列判断正确的是( )
HX
HY
HZ
浓度(mol/L)
0.12
0.2
0.9
1
电离度
0.25
0.1
0.3
0.5
K1
K2
K3
K4
K5
在相同温度,从HX的数据可以说明:
弱电解质溶液,浓度越低,电离度越大,且K1>K2>K3=0.01
室温时,若在NaZ溶液中加水,则c(Z﹣)/[c(HZ)•c(OH﹣)]的比值变小,若加少量盐酸,则比值变大
等物质的量的NaX、NaY和NaZ的混合,c(X﹣)+c(Y﹣)﹣2c(Z﹣)=2c(HZ)﹣c(HX)﹣c(HY),且c(Z﹣)<c(Y﹣)<c(X﹣)
在相同温度下,K5>K4>K3
高中化学选修4第3章水溶液中的离子平衡-解析
一、选择题(共20小题)
分析:
A.电离出来的氢离子浓度越大,与钠反应速率越大;
B.越难电离,则离子越易与氢离子结合;
C.K为甲醇中离子浓度的乘积;
D.根据电荷守恒分析.
解答:
解:
A.电离出来的氢离子浓度越大,与钠反应速率越大,水的电离程度大于甲醇,则水中氢离子浓度大,所以钠与水的反应比钠与甲醇反应更剧烈,故A错误;
B.越难电离,则离子越易与氢离子结合,甲醇难电离,则结合H+的能力CH3O﹣>OH﹣,故B正确;
C.K为甲醇中离子浓度的乘积,则所得到溶液中K=c(CH3O﹣)×
c(CH3OH2+),故C正确;
D.所得到溶液中存在电荷守恒,即c(Na+)+c(CH3OH2+)=c(CH3O﹣),故D错误.
故选BC.
①酸加水稀释,pH升高;
②NH4Cl浓度越小,NH4+水解程度越大;
③NaHCO3溶液显碱性,碳酸氢根离子的水解程度大于电离程度;
④常温下,混合液pH=4,c(H+)=1.0×
10﹣4mol/L,则由Kw可知,c(OH﹣)=1.0×
10﹣10mol/L,由电荷守恒可知,c(CH3COO﹣)﹣c(Na+)=c(H+)﹣c(OH﹣),据物料守恒:
2c(Na+)=c(CH3COOH)+c(CH3COO﹣),据此分析.
①酸加水稀释,pH升高,故错误;
②NH4Cl浓度越小,NH4+水解程度越大,铵根的物质的量相同,0.25mol•L﹣1NH4Cl溶液中铵根水解程度大,故正确;
③NaHCO3溶液显碱性,碳酸氢根离子的水解程度大于电离程度,其离子浓度关系为c(Na+)>c(HCO3﹣)>c(H2CO3)>c(CO32﹣),故错误;
10﹣10mol/L,由电荷守恒可知,Ⅰc(CH3COO﹣)﹣c(Na+)=c(H+)﹣c(OH﹣),据物料守恒:
Ⅱ2c(Na+)=c(CH3COOH)+c(CH3COO﹣),Ⅰ×
2+Ⅱ可得:
c(CH3COO﹣)﹣c(CH3COOH)=2(c(H+)﹣c(OH﹣))=2×
(10﹣4﹣10﹣10)mol/L,故正确;
故选D.
A、醋酸是弱电解质,加水稀释促进醋酸电离;
B、为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH,若pH<7,H2A也可能是弱酸;
C、弱酸的酸性越弱,其酸根离子的水解程度越大;
D、相同温度下,氯化银溶液中存在溶解平衡,溶液中氯离子浓度越大,抑制氯化银溶解程度越大.
A、常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,加水稀释促进醋酸电离,所以稀释后溶液中氢离子浓度大于原来的
,所以溶液的3<pH<4,故A错误;
B、为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH若pH<7,H2A也可能是弱酸,如亚硫酸,故B错误;
C、酸性HF>CH3COOH,物质的量浓度相等的NaF与CH3COOK溶液中,醋酸根离子的水解程度比氟离子强,醋酸根离子浓度小,钾离子与钠离子浓度相等,所以[c(Na+)﹣c(F﹣)]<[c(K+)﹣c(CH3COO﹣)],故C正确;
D、相同温度下,氯化银溶液中存在溶解平衡,溶液中氯离子浓度越大,抑制氯化银溶解程度越大,硝酸银是可溶性盐,所以硝酸银中银离子浓度最大,则银离子浓度大小顺序是:
d>a>b>c,故D错误;
故选C.
A、NaHCO3溶液显碱性;
B、HCN的酸性强于碳酸氢根离子;
C、HCN和HCOOH都是一元酸,相同物质的量时,中和碱的能力相同;
D、根据电荷守恒,c(HCOO﹣)+c(OH﹣)=c(Na+)+c(H+),c(CN﹣)+c(OH﹣)=c(Na+)+c(H+),和水解程度大小分析.
A、NaHCO3溶液中浓度的大小:
c(Na+)>c(HCO3﹣)>c(OH﹣)>c(H+),故A错误;
B、少量的CO2通入到NaCN溶液中:
CN﹣+H2O+CO2=HCN+HCO3﹣,故B错误;
C、等浓度、等体积的HCOOH和HCN,n(HCN)=n(HCOOH),中和酸需要碱的物质的量与酸的物质的量、酸的元数成正比,所以中和等体积、等浓度的HCOOH和HCN消耗NaOH的量前者等于后者,故C正确;
D.根据电荷守恒,c(HCOO﹣)+c(OH﹣)=c(Na+)+c(H+),c(CN﹣)+c(OH﹣)=c(Na+)+c(H+),即离子总数是n(Na+)+n(H+)的2倍,而NaCN的水解程度大,即NaCN溶液中的c(OH﹣)大,c(H+)小,c(Na+)相同,所以甲酸钠中离子浓度大,故D错误;
A.pH相同的三种酸性溶液,由图象可知,a的pH变大,b的pH不变,c的pH减小,则露置于空气中一段时间,a可能被氧化,b为不挥发的强酸,c中氢离子浓度增大,以此来解答;
B.乙酸为弱电解质,与氨气反应生成醋酸铵为强电解质;
C.Cu与浓硝酸反应生成二氧化氮,与稀硝酸反应生成NO;
D.△H=正反应的活化能﹣逆反应的活化能.
A.H2S溶液被氧化生成水和S,其pH增大,稀H2SO4溶液不发生变化,其pH不变,而H2SO3溶液被氧化生成硫酸,氢离子浓度增大,其pH减小,与图象一致,故A正确;
B.乙酸为弱电解质,溶液的导电能力较弱,与氨气反应生成醋酸铵为强电解质,溶液的导电能力增强,图中曲线变化趋势错误,故B错误;
C.铜先和浓硝酸反应生成二氧化氮气体,随着反应的进行,浓硝酸变成稀硝酸,铜和稀硝酸反应生成一氧化氮,当硝酸完全反应时,生成的气体为定值,故C正确;
D.△H=正反应的活化能﹣逆反应的活化能,则合成甲醇的热化学方程式为CO(g)+2H2(g)=CH3OH(g)△H=﹣(b﹣a)kJ•mol﹣1,故D正确.
故选B.
根据盐酸和醋酸溶液中的氢离子物质的量和加入锌的物质的量,依据盐酸是强酸,醋酸是弱酸存在电离平衡判断反应过程和反应量的关系,结合图象中的纵坐标和横坐标的意义,曲线的变化趋势,起点、拐点、终点的意义分析判断是否符合事实.
体积都为1L,pH都等于2的盐酸和醋酸溶液中,n(CH3COOH)>n(HCl)=0.01mol,锌和酸反应Zn+2H+=Zn2++H2↑,盐酸酸溶液中氢离子不足,醋酸溶液中存在电离平衡,平衡状态下的氢离子不足,但随着反应进行,醋酸又电离出氢离子进行反应,放出的氢气一定比盐酸多,开始时由于氢离子浓度相同,开始的反应速率相同,反应过程中醋酸溶液中的氢离子浓度始终比盐酸溶液中的氢离子浓度大,所以反应速率快;
反应后,醋酸有剩余,导致醋酸溶液中pH小于盐酸溶液中;
A.由于醋酸会不断电离出H+,因此醋酸pH上升会比盐酸慢.虽然和同量的Zn反应,醋酸速率快,但是这是pH,不是氢气的量,所以pH上升醋酸慢,故A错误;
B.反应开始氢离子浓度相同,反应速率相同.曲线从相同速率开始反应,但醋酸溶液中存在电离平衡,反应过程中醋酸溶液中的氢离子浓度始终比盐酸溶液中的氢离子浓度大,所以醋酸溶液反应过程中反应速率快,溶解的锌的量也比盐酸多,所以图象不符合题意,故B错误;
C.产生氢气的量从0开始逐渐增多,最终由于醋酸电离平衡的存在,生成氢气的量比盐酸多,反应过程中氢离
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学选修4 第3章 水溶液中的离子平衡 解析 高中化学 选修 水溶液 中的 离子 平衡
 冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《d t n l》公开课教案优秀教学设计5.docx
《d t n l》公开课教案优秀教学设计5.docx
